Cloning and expression analysis of PCNA in Metapenaeus affinis
-
摘要: 增殖细胞核抗原 (Proliferating cell nuclear antigen, PCNA) 作为DNA聚合酶δ的辅助蛋白,在DNA复制过程中发挥重要作用。近缘新对虾 (Metapenaeus affinis) 卵巢发育过程中存在细胞增殖活动旺盛的阶段,但目前关于其卵巢发育的分子机制研究较少。利用RACE (Rapid amplification of cDNA ends) 技术获得近缘新对虾PCNA (MaPCNA) 基因的cDNA序列全长,并通过实时荧光定量PCR (qRT-PCR) 对其进行卵巢发育相关的表达分析。MaPCNA全长为1 144 bp,包含140 bp的5'非编码区,221 bp的3'非编码区,开放阅读框 (ORF) 为783 bp,编码260个氨基酸。MaPCNA蛋白的相对分子质量为28.82 kD,理论等电点为4.5。多重比对分析表明,PCNA氨基酸序列在甲壳动物中较为保守。组织表达结果显示,MaPCNA基因在检测的组织中均有表达,其中在卵巢中的表达量最为显著 (P<0.05)。在不同发育阶段的卵巢中,MaPCNA基因的表达出现变化 (P<0.05),从I期开始逐渐上升,到III期表达量最高,之后显著降低并趋于平稳。MaPCNA基因在幼体发育不同时期的表达呈现出一定的规律性趋势,在受精卵时期的表达量最高,之后呈下降趋势,从无节幼体VI期开始表达平稳。研究结果提示PCNA基因可能在近缘新对虾的卵巢发育过程中发挥重要作用。Abstract: As a coprotein of DNA polymerase δ, proliferating cell nuclear antigen (PCNA) plays an important role in the process of DNA replication. There is a stage of vigorous cell proliferation during the ovarian development in Metapenaeus affinis, but little attention has been paid to its molecular mechanism. In this study, we applied rapid amplification of cDNA ends (RACE) technique to obtain the full length cDNA sequences of PCNA in M. affinis (MaPCNA), and analyzed the expression of MaPCNA related to ovarian development by real-time fluorescent quantitative PCR (qRT-PCR). The total length of MaPCNA was 1 144 bp, including 140 bp of 5' untranslated region, 221 bp of 3' untranslated region and 783 bp ORF encoding 260 amino acids. The molecular mass of MaPCNA protein was 28.82 kD and the theoretical isoelectric point was 4.5. The protein homology analysis shows that MaPCNA had high homology with other crustaceans. The result of tissue expression shows that Ma-PCNA was expressed in all tested tissues, with the highest expression in ovary (P<0.05). The expression of MaPCNA in ovary at different developmental stages showed significant changes (P<0.05), increasing from stage I to stage III gradually, decreasing significantly and then tending to be stable. The expression of MaPCNA showed a regular change trend at different larval developmental stages. The expression level of MaPCNA was the highest in oosperm, then began to decline, and became stable from the Nauplius VI. The results suggest that PCNA may play an important role in the ovarian development of M. affinis.
-
Keywords:
- Metapenaeus affinis /
- PCNA /
- Cloning /
- Gene expression
-
增殖细胞核抗原 (Proliferating cell nuclear antigen, PCNA) 在1978年系统性红斑狼疮患者的血清中被发现,因其在分裂的细胞核中表达而得名[1]。与此同时,Bravod和Celis [2]在细胞周期的S期中发现了一种蛋白,称为cyclin,之后被证实是PCNA。PCNA属于滑动夹子家族成员,深入研究发现PCNA基因在真核生物染色体DNA复制过程中起关键作用,其作为DNA聚合酶δ的“DNA滑动钳”,围绕引物进行组装,之后跟聚合酶结合,从而调节细胞的增殖[3-4]。此外,PCNA基因与相关蛋白质相互作用,参与调控细胞修复、细胞周期、细胞凋亡、染色体组装等过程[5-6]。在脊椎动物中,PCNA基因通过调控牦牛 (Bos mutus) 睾丸间质细胞的分裂和精母细胞的增生进而影响精子的发生[7]。在小鼠 (Mus musculus) 的卵巢中,PCNA基因通过促进卵母细胞的凋亡来调节原始卵泡组装[8],是卵泡发育过程中的关键调节因子。
PCNA基因从G1期开始积累,到S期表达量最高,之后在G2/M期减少,这种在细胞周期中的合成和表达动态变化有助于研究物种的发育过程。迄今为止,已在凡纳滨对虾 (Litopenaeus vannamei) [9]、中国明对虾 (Fenneropenaeus chinensis) [10]、日本囊对虾 (Marsupenaeus japonicus) [11]、中华绒螯蟹 (Eriocheir sinensis) [12]、斑节对虾 (Penaeus monodon) [13]、克氏原螯虾 (Procambarus clarkii) [14]等多种甲壳动物中分离鉴定出PCNA基因。但该基因在近缘新对虾 (Metapenaeus affinis) 中的研究尚未见报道。
近缘新对虾隶属于对虾科、新对虾属,俗称麻虾、砂虾,在广东沿岸海域均有分布,是广东海区重要的经济虾类之一,其肉质饱满、营养丰富,含有较多蛋白质、矿物质和饱和脂肪酸等[15-16]。近缘新对虾广泛栖息在5~55 m深的砂质或泥底质海域,因而可成为监测海域生态系统污染源的合适物种[17-18]。雌虾一年四季均有产卵,繁殖的高峰期因地理位置的不同而有所差异[19-20]。关于近缘新对虾的研究主要集中于不同海域的渔业资源、种群动态与繁殖特征[21-23],而有关遗传育种与生殖发育等方面的研究较少。目前近缘新对虾亲虾全部来源于野生资源,由于过度捕捞,已导致野生亲虾资源严重枯竭,制约了其养殖产业的发展[24]。突破近缘新对虾亲虾全人工培育是该产业迫切需要解决的问题,而阐明其性腺发育调控机制是攻克近缘新对虾亲虾全人工繁育的关键。为探究PCNA基因在近缘新对虾性腺中的功能机制,在前期转录组测序结果[24]的基础上得到PCNA基因的cDNA片段。本研究利用RACE技术获得PCNA基因的cDNA序列全长,分析了PCNA基因在转录水平上的表达特征,为探讨PCNA基因在性腺发育中的功能及进一步研究近缘新对虾性腺发育的分子机制提供基础数据。
1. 材料与方法
1.1 实验材料
本研究所使用的近缘新对虾来源于中国水产科学研究院南海水产研究所深圳试验基地,体质量为 (10±2) g,水温为 (28±1) ℃,实验前放于充氧的海水中暂养3 d。随机选取3尾健康、完好的近缘新对虾雌虾,解剖取肝胰腺、鳃、肠、胃、心脏、肌肉、神经、卵巢等组织并于液氮中速冻,之后保存于−80 ℃超低温冰箱。
根据外观特征,将近缘新对虾卵巢分为I期 (增殖期:透明,小卵巢)、II期 (发育早期:乳白色)、III期 (发育期:黄色)、IV期 (将成熟期:浅绿色)、V期 (成熟期:暗绿色)、VI期 (枯竭期:半透明)。近缘新对虾幼体发育时期的材料,根据形态学特征[25-26],在夏季育苗期间采集,包括受精卵时期 (O:卵子呈绿色)、无节幼体I期 (NI:尾棘1对,第一对附肢前端刚毛等长)、无节幼体II期 (NII:尾棘1对,第一对附肢前端刚毛显著长于其他刚毛)、无节幼体III期 (NIII:尾棘3对,腹部出现附肢生长芽突)、无节幼体IV期 (NIV:尾棘4对)、无节幼体V期 (NV:尾棘5对,身体拉长,出现头胸节的雏形)、无节幼体VI期 (NVI:尾棘7对,头胸节显著)、溞状幼体I期 (ZI:体分节,分头胸部与腹部)、溞状幼体II期 (ZII:复眼柄生成,尾节无尾肢)、溞状幼体III期 (ZIII:出现尾肢)、糠虾I期 (MI:五对步足长出外肢)、糠虾II期 (MII:腹部出现短小的游泳足)、糠虾III期 (MIII:腹部游泳足出现分节)、仔虾1 d (P1:开始水平游动)。
1.2 MaPCNA基因的克隆
使用HiPure Total RNA Plus Kits (Magen,广州) 提取近缘新对虾卵巢组织总RNA,1% (质量分数)琼脂糖凝胶电泳检测RNA的完整性,通过Nanodrop (Thermo,美国) 检验RNA的浓度与纯度。使用SMARTer® RACE 5'/3' Kit (TaKaRa,日本) 制备cDNA模板。在MaPCNA基因已验证序列的基础上设计5'和3'末端的扩增引物 (表1)。PCR扩增获得的目的片段进行1% (质量分数)琼脂糖凝胶电泳,之后使用FastPure Gel DNA Extraction Mini Kit (Vazyme,南京) 进行凝胶回收纯化目的片段。纯化产物与pMD19-T载体连接,导入DH-5α感受态细胞筛选阳性克隆进行测序。通过DNAMAN 9软件对MaPCNA基因的中间cDNA序列、5'和3'末端cDNA序列进行拼接,进而获得MaPCNA基因的cDNA全长序列。引物合成由北京睿博兴科生物技术有限公司完成,测序在北京六合华大基因科技有限公司进行。
表 1 实验所使用的引物序列Table 1. Oligonucleotide primers used in experiment引物
Primer引物序列 (5'—3')
Primer sequence (5'−3')用途
FunctionMaPCNA-F GGAAGTCTGTTGAAGAAGGTGTTGGA 验证序列 MaPCNA-R GTATTCTGCCACAAAGCCATAGTAAGC MaPCNA-5GSP1 TTTGGACATGCTGGTGAGGTTCATGCCC 5'RACE MaPCNA-5GSP2 CATGCCCATGATGAGGTTTCGGTCGC MaPCNA-3GSP1 AAAGCAACACCCCTTTCCCCACAGG 3'RACE MaPCNA-3GSP2 TCCCTGTCCATGTCTCCTGATGTACCCC UPM-long CTAATACGACTCACTATAGGGCAAGCAGTGGTATCAACGCAGAGT RACE UPM-short CTAATACGACTCACTATAGGGC NUP AAGCAGTGGTATCAACGCAGAGT MaPCNA-qF TCATCGAGATGCAGGAGCCAGTTA qPCR MaPCNA-qR ATCAGGAGACATGGACAGGGAGAC EF-1α-qF AAGCCAGGTATGGTTGTCAACTTT 内参 EF-1α-qR CGTGGTGCATCTCCACAGACT 1.3 MaPCNA基因的生物信息学分析
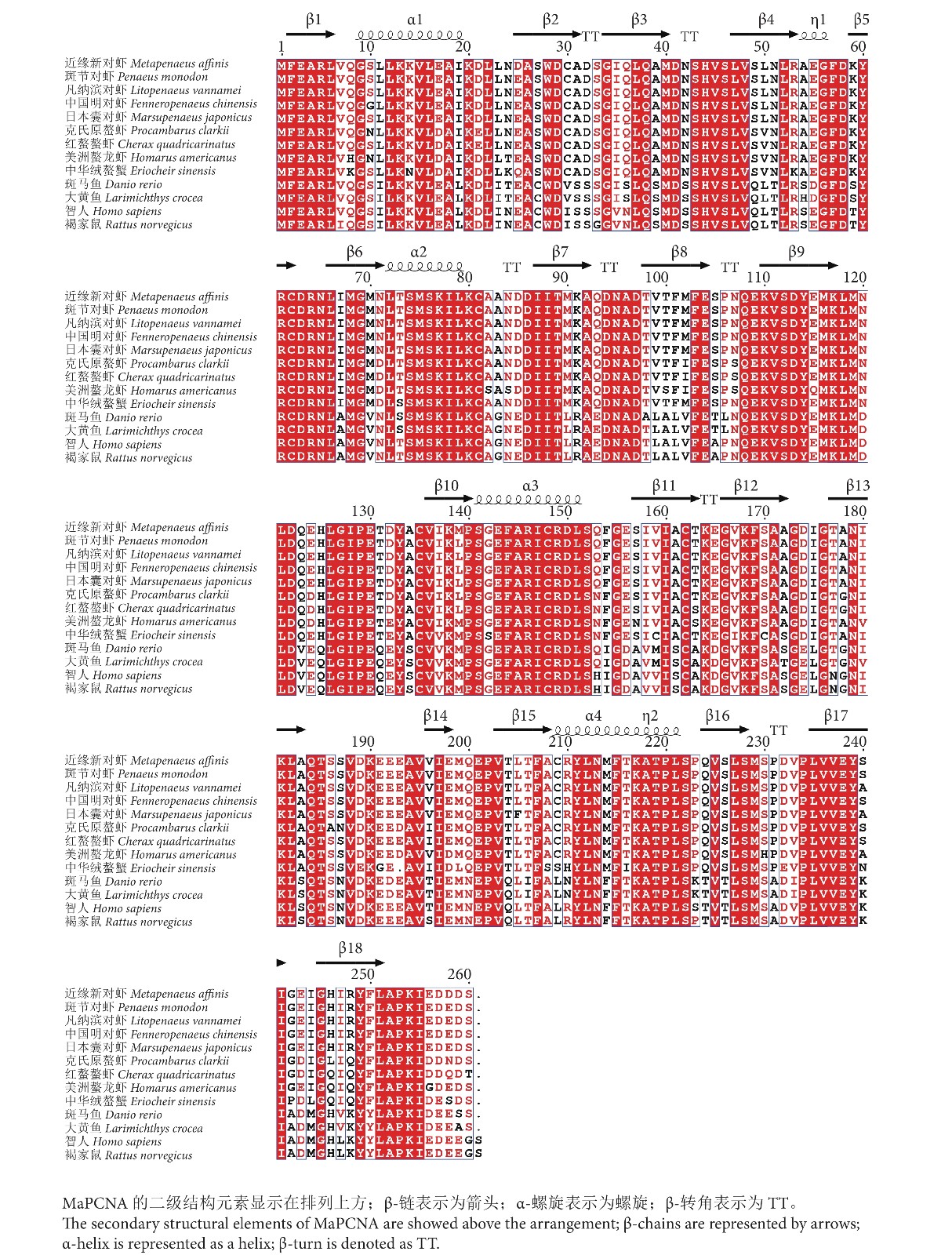
BLAST在线网站 (http://www.ncbi.nlm.nih.gov/BLAST/) 比对PCNA的核苷酸序列以及蛋白序列的相似性;ORF-Finder (https://www.ncbi.nlm.nih.gov/orffinder/) 查找开放阅读框 (Open Reading Frame, ORF);在线网站进行信号肽的预测[27] (https://services.healthtech.dtu.dk/service.php?SignalP-5.0);亚细胞定位预测使用Cell-PLoc 2.0服务器[28] (http://www.csbio.sjtu.edu.cn/bioinf/Cell-PLoc-2/)。通过在线服务器NetNGlyc 1.0 Server[29] (https://services.healthtech.dtu.dk/service.php?NetNGlyc-1.0) 预测糖基化位点;在NetPhos 3.1 Server[30] (https://services.healthtech.dtu.dk/service.php?NetPhos-3.1) 预测磷酸化位点;蛋白质亲水性与疏水性预测使用ProtScale[31] (https://www.expasy.org/resources/protscale);使用在线服务器TMHMM-2.0[32] (https://services.healthtech.dtu.dk/service.php?TMHMM-2.0) 预测跨膜结构;Pfam 35.0[33] (http://pfam.xfam.org/) 用于进行蛋白结构域的分析;蛋白质二级结构预测使用SOPMA软件[34] (https://npsa-prabi.ibcp.fr/cgi-bin/npsa_automat.pl?page=npsa_sopma.html);蛋白质三级结构预测使用在线服务器SWISS-MODEL[35] (https://swissmodel.expasy.org/)。通过BLAST网站下载13个物种的PCNA氨基酸序列,包括甲壳纲的斑节对虾 (XP_037796602.1)、凡纳滨对虾 (AEP83535.1)、中国明对虾 (ABM66815.1)、日本囊对虾 (ACA09718.1)、克氏原螯虾 (XP_045620914.1)、红螯螯虾 (Cherax quadricarinatus, QBK50993.1)、美洲螯龙虾 (Homarus americanus, XP_042224267.1) 与中华绒螯蟹 (XP_050721402.1);硬骨鱼纲的斑马鱼 (Danio rerio, NP_571479.2) 与大黄鱼 (Larimichthys crocea, XP_010732529.1);哺乳纲的智人 (Homo sapiens, NP_002583.1) 与褐家鼠 (Rattus norvegicus, NP_071776.1),之后使用Clustal X[36]和ESPript 3.0[37]构建基于蛋白质序列的多重序列比对图谱;用MEGA 7[38] 构建MaPCNA系统进化树。
1.4 MaPCNA基因的表达特征分析
使用Evo M-MLV RT Mix Kit with gDNA Clean for qPCR (AG,广州) 制备实时荧光定量 PCR (qRT-PCR) 的cDNA模板,根据SYBR® Green Premix Pro Taq HS qPCR Kit (AG,广州) 说明书配制反应体系 (12.5 μL) :包含2×SYBR Premix Ex Taq 6.25 μL、上下游引物各0.5 μL、cDNA模板1.0 μL以及去离子水4.25 μL。EF-1α作为内参,每个样品重复3次。PCR反应程序为:95 ℃ 5 min;95 ℃ 10 s,60 ℃ 30 s,40个循环。根据2−ΔΔCT法分析PCNA基因的表达,实验数据用“平均值±标准差 (
$\overline x \pm {{s}}$ )”表示,采用SPSS 23.0软件[39]进行单因素方差分析,用Origin 2021软件[40]绘制柱状图。2. 结果
2.1 MaPCNA基因的序列分析
MaPCNA基因的cDNA序列全长为1 144 bp,包含140 bp 的5'非编码区 (UTR) 以及221 bp的3'UTR,ORF 为783 bp,编码260个氨基酸 (图1)。MaPCNA蛋白的相对分子质量为28.82 kD,理论等电点为4.5,为亲水性蛋白。氨基酸序列分析显示,有24 个磷酸化位点,分别为15个丝氨酸位点 (S)、6个苏氨酸位点 (T) 和3个酪氨酸 (Y) 位点。没有预测到信号肽序列,表明MaPCNA蛋白为非分泌蛋白。NetNGlyc 1.0 Server预测MaPCNA蛋白有一个N-糖基化位点,位于第71位氨基酸。Cell-PLoc 2.0预测MaPCNA蛋白的亚细胞定位于细胞核中。在线软件TMHMM分析MaPCNA蛋白中未见明显跨膜区域,表明其为非跨膜蛋白。软件Pfam 35.0分析结果显示 MaPCNA蛋白由N-端结构域 (1—125 aa)、域间连接环 (Interdomain connecting loop, IDCL) (121—133 aa) 及C-端结构域 (127—254 aa) 组成。
2.2 MaPCNA基因的结构与氨基酸序列多重比对
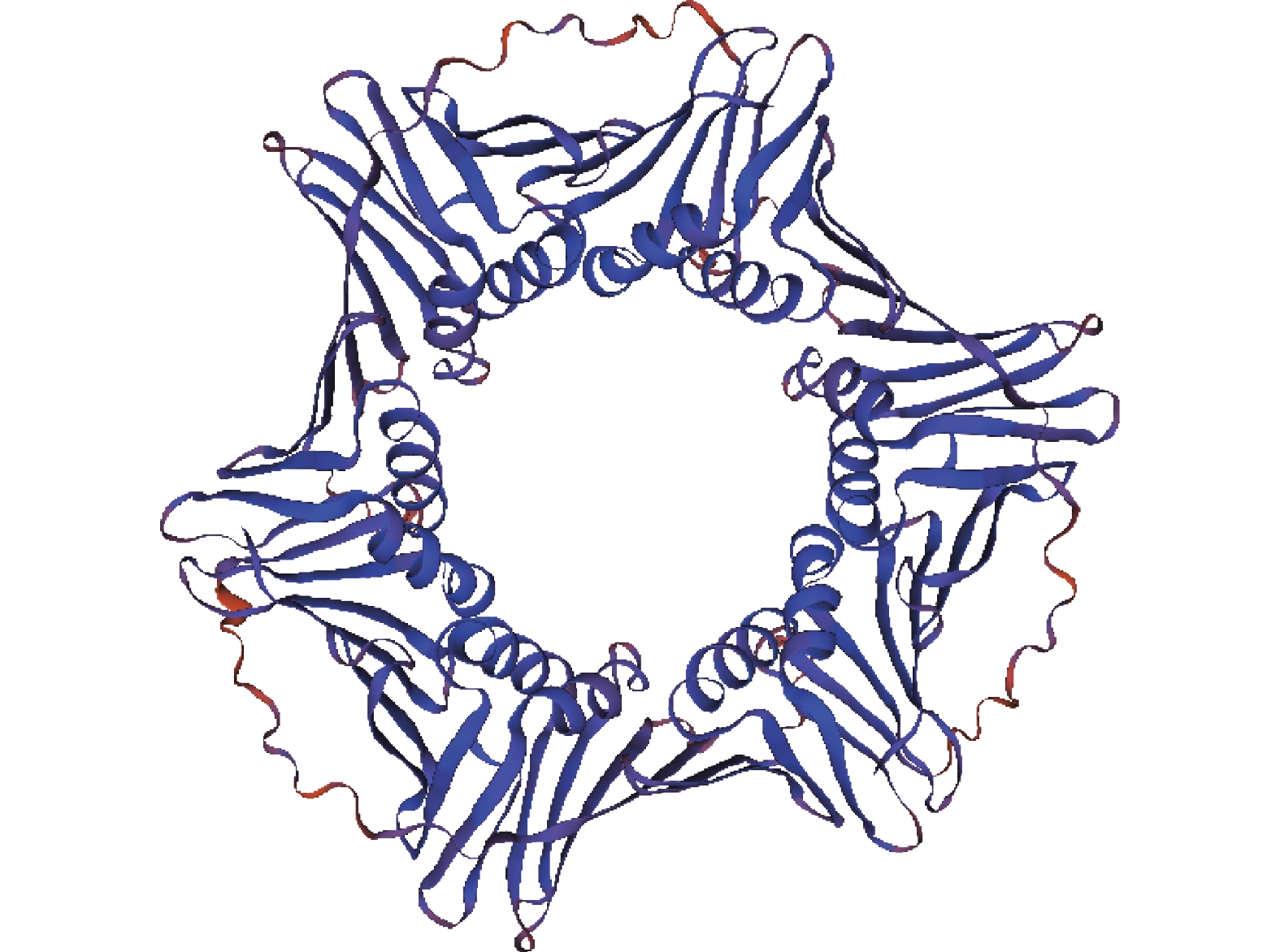
MaPCNA蛋白二级结构中无规则卷曲、α-螺旋、β-转角和β-折叠占比分别为38.08%、29.62%、5.00%和27.31%,包含4个 α螺旋和1个扭曲的 β-折叠,β-折叠由 18个反向平行的 β折叠股构成 (图2)。N-端结构域由α-螺旋 1、2和 1—9号的β折叠股构成,C-端结构域则是由α螺旋 3、4和10—18号的β折叠股构成,而域间连接环将N-端结构域与C-端结构域连接起来。MaPCNA蛋白的三维结构由构象相似的3个单体头尾相连,每个单体包含2个相似球状的结构域,以及2个结构域之间长的卷曲的环状结构,从而形成一个伪六重轴对称结构,是一个对称的同源三聚体 (图3)。
多重比对结果显示,MaPCNA氨基酸序列与甲壳纲中8个物种的PCNA氨基酸序列同一性较高,其中最高的是斑节对虾 (98.85%),其次是凡纳滨对虾与中国明对虾 (均为98.46%)、日本囊对虾 (98.08%)、中华绒螯蟹 (85.77%);与斑马鱼和大黄鱼的同一性均为70.38%;MaPCNA氨基酸序列与智人 (73.75%) 和褐家鼠 (73.36%) 的同一性较低 (图2)。这表明PCNA在各物种间较为保守,并在甲壳动物中高度保守。
2.3 MaPCNA基因的系统发育分析
利用MEGA 7软件基于邻接法 (Neighbor-Joining, NJ) 法构建PCNA氨基酸序列系统进化树 (图4)。进化树分为两大类,MaPCNA单独聚为一支,之后与凡纳滨对虾、日本囊对虾聚为一小支,再与盲虾 (Rimicaris exoculata, ATY70175.1)、美洲螯龙虾 (XP_042224267.1)、红螯螯虾 (QBK50993.1)、克氏原螯虾、沙蚕 (Trinorchestia longiramus, KAF2350181.1),端足虫 (Hyalella azteca, XP_018017642.1) 等甲壳纲物种聚为一类。长叶异痣蟌 (Ischnura elegans, XP_046392856.1)、德国小蠊 (Blattella germanica, PSN38108.1)、内华达古白蚁 (Zootermopsis nevadensis, XP_021934966.1)、棕榈蓟马 (Thrips palmi, XP_034249598.1)、褐透翅尖叶蝉 (Homalodisca vitripennis, XP_046665545.1) 等昆虫纲物种聚为一类。这说明该基因在节肢动物进化过程中较为保守。
2.4 MaPCNA基因在不同组织中的表达分析
本研究检测了PCNA 基因在近缘新对虾的肝胰腺、鳃、肠、胃、心脏、肌肉、眼脑神经、胸腹神经、卵巢组织中的表达情况,结果显示MaPCNA基因在所检测的组织中均有表达,其中在卵巢中的表达量最高 (P<0.05),其次是心脏和鳃,而在肠、肌肉、眼脑神经、胃、肝胰腺和胸腹神经中的表达量较低 (图5)。
![]() 图 5 MaPCNA 基因在不同组织中的相对表达量注:图中数值为“平均值±标准差”(n=3),小写字母不同表示各组之间具有显著差异 (P<0.05);后图同此。Figure 5. Relative expression of MaPCNA gene in different tissuesNote: The values are "$ {\rm{Mean}} \pm {\rm{SD}}$" (n=3). Different lowercase letters indicate significant difference among groups (P<0.05); the same case in the following figures.
图 5 MaPCNA 基因在不同组织中的相对表达量注:图中数值为“平均值±标准差”(n=3),小写字母不同表示各组之间具有显著差异 (P<0.05);后图同此。Figure 5. Relative expression of MaPCNA gene in different tissuesNote: The values are "$ {\rm{Mean}} \pm {\rm{SD}}$" (n=3). Different lowercase letters indicate significant difference among groups (P<0.05); the same case in the following figures.2.5 MaPCNA基因在卵巢发育不同阶段的表达分析
通过检测近缘新对虾卵巢发育6个时期中MaPCNA基因的表达变化,显示MaPCNA在卵巢发育过程中发生了显著变化,增殖期的I期与发育初期的II期中MaPCNA基因的表达量没有差异,到发育期的III期表达量显著升高,之后开始下降并在成熟期的V期与枯竭期的VI期保持平稳 (图6)。
2.6 MaPCNA基因在幼体发育各阶段的表达分析
MaPCNA基因在幼体发育不同阶段的表达显示,在受精卵时期的表达量显著高于其他阶段,在无节幼体I期显著下降 (P<0.05),到无节幼体II期上升,之后在无节幼体VI期再一次显著下降,直至仔虾期均无显著变化 (图7)。总体而言,MaPCNA基因在幼体发育阶段中的表达呈下降趋势。
3. 讨论
当生物体内进行DNA复制或DNA修复时,PCNA被多亚单位复制因子C (夹钳装载器) 装载到复制的DNA链上,形成包围DNA的同源三聚体形式的DNA夹钳,而这种三聚体形式的PCNA在前链和后链DNA合成过程中充当DNA聚合酶δ的加工因子[41]。MaPCNA氨基酸序列由N-端结构域、C-端结构域以及域间连接环组成。域间连接环作为最主要的蛋白结合位点,与DNA复制相关的蛋白质如p21、DNA聚合酶δ、末端内切酶I和连接酶I等结合,协调完成不同的调控过程[42],这说明MaPCNA与其他物种的PCNA[7]一样,在细胞周期调控中起着重要作用。多重比对发现MaPCNA与其他甲壳动物的PCNA氨基酸序列有较高的同源性,其中与斑节对虾的同一性最高。PCNA氨基酸序列的高度保守,暗示MaPCNA与其他甲壳动物中的PCNA可能具有类似的功能。
MaPCNA基因在所检测的组织中均有表达,在卵巢组织中的表达量显著高于其他组织,表明PCNA基因可能参与了近缘新对虾卵巢的发育。相关研究发现PCNA基因在中国明对虾[10]、斑节对虾[13]和长牡蛎 (Crassostrea gigas) [43]的性腺组织中高度表达,而凡纳滨对虾中的PCNA基因在肌肉中的表达量显著高于其他组织[9]。以上研究表明,甲壳类的PCNA基因在性腺、肌肉等高度活跃的增殖组织中表达量高。此外,有研究发现在细胞周期的S期存在一个有活性的PCNA-CDK-Cyclin复合物[44],PCNA基因在其中的作用主要是充当CDK及其底物之间的桥梁,说明PCNA基因作为细胞周期的调控因子参与了细胞的增殖生长与相关的转录调控过程。MaPCNA基因在心脏组织中存在较高的表达量可能与近缘新对虾不同生长阶段的细胞活性有关。
已有研究表明PCNA mRNA在活跃的增殖细胞中高度表达[11,13],而MaPCNA基因在卵巢组织中的表达量显著高于其他组织,因此开展卵巢不同发育阶段MaPCNA 基因的表达分析将有助于进一步了解近缘新对虾的卵巢发育机制。本研究结果显示,MaPCNA基因在卵巢发育不同阶段中的表达量存在显著性差异,I期与II期是近缘新对虾卵巢发育的初期,此时存在大量增殖的卵原细胞,因而MaPCNA基因的表达量开始升高,到III期达到最高,IV期的卵巢已初步成熟,细胞的增殖活性降低,MaPCNA基因的表达量也随之下降。这与斑节对虾[13]和牡蛎[45]中的表达模式相似。在其他生物中也有类似结果,在小鼠卵巢中PCNA基因的表达水平随着卵巢的发育而显著降低[8]。在高等植物中PCNA基因在发育早期的表达量较高,但在成熟时期的表达量降低[46]。PCNA基因在成熟卵巢中的表达量减少,可能表明成熟时期的DNA复制达到了稳定水平,细胞增殖活动减缓,因而PCNA基因的表达量降低。但也有其他物种的PCNA基因在卵巢中的表达模式不同,尼罗罗非鱼 (Oreochromis niloticus) 卵巢发育的初次和早期二次生长期间的PCNA基因高度表达,而卵母细胞生成期间PCNA基因的表达量下降[47];PCNA基因的表达量在银鲑 (Oncorhynchus kisutch) 卵巢发育不同阶段的卵泡中稳步降低[48],这说明PCNA的调节机制可能因mRNA和蛋白质合成不同而存在种间差异。研究显示,斑马鱼卵泡上皮的卵母细胞发育过程中PCNA阳性细胞的数量不断增加,其中在卵黄形成卵泡中最多[49]。与斑马鱼相似,本研究中MaPCNA基因在III期卵巢组织的表达量最高。III期卵巢是近缘新对虾卵巢的发育期,此时卵巢开始快速发育,并且出现卵黄颗粒。而在III期的高表达量可能提示MaPCNA基因在卵巢快速发育及卵黄形成中扮演重要角色。
为了分析近缘新对虾幼体不同发育阶段中PCNA基因表达的变化,本研究检测了近缘新对虾不同发育阶段,包括受精卵、六期无节幼体、三期溞状幼体、三期糠虾期和仔虾期MaPCNA基因的表达情况。在受精后24 h的斑马鱼胚胎中检测到PCNA 基因大量表达[50],与MaPCNA基因在受精卵时期的高表达相似,这可能是受精卵细胞的快速卵裂增殖所致。Peng等[12]研究显示中华绒螯蟹在不同幼体阶段PCNA基因的表达量显著不同,在大眼幼体阶段表达量较低,一期仔蟹阶段表达量最高,到三期仔蟹阶段显著降低,一期仔蟹阶段PCNA基因的高表达表明PCNA基因可能在中华绒螯蟹的短尾发育过程中具有关键作用。研究发现在大鼠胚胎的生殖细胞中,PCNA基因大量存在,出生后的表达显著降低[51],而敲除PCNA基因的小鼠,子代中产生早期胚胎细胞致死的表型[52],这提示PCNA基因对于胚胎发育的重要性。在近缘新对虾的幼体发育过程中,在无节幼体时期身体开始拉长,显现头胸节雏形,MaPCNA基因的大量存在暗示其可能参与了近缘新对虾幼体的体节增长及头胸节形成过程,推测PCNA基因在近缘新对虾幼体发育的早期阶段发挥着重要作用。
-
图 5 MaPCNA 基因在不同组织中的相对表达量
注:图中数值为“平均值±标准差”(n=3),小写字母不同表示各组之间具有显著差异 (P<0.05);后图同此。
Figure 5. Relative expression of MaPCNA gene in different tissues
Note: The values are "$ {\rm{Mean}} \pm {\rm{SD}}$" (n=3). Different lowercase letters indicate significant difference among groups (P<0.05); the same case in the following figures.
表 1 实验所使用的引物序列
Table 1 Oligonucleotide primers used in experiment
引物
Primer引物序列 (5'—3')
Primer sequence (5'−3')用途
FunctionMaPCNA-F GGAAGTCTGTTGAAGAAGGTGTTGGA 验证序列 MaPCNA-R GTATTCTGCCACAAAGCCATAGTAAGC MaPCNA-5GSP1 TTTGGACATGCTGGTGAGGTTCATGCCC 5'RACE MaPCNA-5GSP2 CATGCCCATGATGAGGTTTCGGTCGC MaPCNA-3GSP1 AAAGCAACACCCCTTTCCCCACAGG 3'RACE MaPCNA-3GSP2 TCCCTGTCCATGTCTCCTGATGTACCCC UPM-long CTAATACGACTCACTATAGGGCAAGCAGTGGTATCAACGCAGAGT RACE UPM-short CTAATACGACTCACTATAGGGC NUP AAGCAGTGGTATCAACGCAGAGT MaPCNA-qF TCATCGAGATGCAGGAGCCAGTTA qPCR MaPCNA-qR ATCAGGAGACATGGACAGGGAGAC EF-1α-qF AAGCCAGGTATGGTTGTCAACTTT 内参 EF-1α-qR CGTGGTGCATCTCCACAGACT -
[1] MIYACHI K, FRITZLER M J, TAN E M. Autoantibody to a nuclear antigen in proliferating cells[J]. J Immunol, 1978, 121(6): 2228-2234. doi: 10.4049/jimmunol.121.6.2228
[2] BRAVO R, CELIS J E. A search for differential polypeptide synthesis throughout the cell cycle of HeLa cells[J]. J Cell Biol, 1980, 84(3): 795-802. doi: 10.1083/jcb.84.3.795
[3] SCHRECKER M, CASTABEDA J C, DEVBHANDARI S, et al. Multistep loading of a DNA sliding clamp onto DNA by replication factor C[J]. ELIFE, 2022, 11: e78253. doi: 10.7554/eLife.78253
[4] GONZALEZ-MAGANA A, BLANCO F J. Human PCNA structure, function, and interactions[J]. Biomolecules, 2020, 10(4): 570. doi: 10.3390/biom10040570
[5] YOUNG P S, JEONG M S, CHANG W H, et al. Structural and functional insight into proliferating cell nuclear antigen[J]. J Microbiol Biotechnol, 2016, 26(4): 637-647. doi: 10.4014/jmb.1509.09051
[6] NAIR A G, RABAS N, LEJON S, et al. Unorthodox PCNA binding by chromatin assembly factor 1[J]. Int J Mol Sci, 2022, 23(19): 11099. doi: 10.3390/ijms231911099
[7] 李忠邦. LYZL4, LYZL6和PCNA在牦牛睾丸中的表达定位及组织学分析[D]. 兰州: 西北民族大学, 2019: 22-39. [8] XU B, HUA J, ZHANG Y W, et al. Proliferating Cell Nuclear Antigen (PCNA) regulates primordial follicle assembly by promoting apoptosis of oocytes in fetal and neonatal mouse ovaries[J]. PLoS One, 2017, 6(1): e16046.
[9] MUHAMMAD F. Ontogenesis of main organs and cloning and expression of two immune-related genes in Litopenaeus vannamei[D]. 青岛: 中国海洋大学, 2012: 78-88. [10] XIE Y S, WANG B, LI F H, et al. Molecular cloning and characteri-zation of proliferating cell nuclear antigen (PCNA) from Chinese shrimp Fenneropenaeus chinensis[J]. Comp Biochem Physiol B, 2008, 151: 225-229. doi: 10.1016/j.cbpb.2008.07.006
[11] ZHANG Z P, SHEN B L, WANG Y L, et al. Molecular cloning of proliferating cell nuclear antigen and its differential expression analysis in the developing ovary and testis of penaeid shrimp Marsupenaeus japonicus[J]. DNA Cell Biol, 2010, 29: 163-170. doi: 10.1089/dna.2009.0958
[12] PENG L, JIE Z, YI K, et al. Identification, mRNA expression and characterization of proliferating cell nuclear antigen gene from Chinese mitten crab Eriocheir sinensis[J]. Comp Biochem Physiol A, 2010, 157(2): 170-176. doi: 10.1016/j.cbpa.2010.06.163
[13] 王成扬, 赵超, 傅明骏, 等. 斑节对虾增殖细胞核抗原基因克隆及表达分析[J]. 中国水产科学, 2016, 23(5): 1052-1062. [14] 姜虎成. 克氏原螯虾转录组测序数据发掘和性腺发育相关基因功能初步研究[D]. 上海: 上海海洋大学, 2015: 43-63. [15] 杨亚男, 黄辉洋, 尚丽丽, 等. 近缘新对虾Cyclin B基因的克隆与原核表达[J]. 水产学报, 2013, 37(2): 184-191. [16] DINCER T, AYDIN İ. Proximate composition and mineral and fatty acid profiles of male and female jinga shrimps (Metapenaeus affinis, H. Milne Edwards, 1837)[J]. Turk J Vet Anim Sci, 2014, 38: 445-451. doi: 10.3906/vet-1301-15
[17] KESHAVARZIFARD M, VAZIRZADEH A, SHARIFINIA M. Occurrence and characterization of microplastics in white shrimp, Metapenaeus affinis, living in a habitat highly affected by anthropogenic pressures, northwest Persian Gulf[J]. Mar Pollut Bull, 2021, 169: 112581. doi: 10.1016/j.marpolbul.2021.112581
[18] KESHAVARZIFARD M, VAZIRZADEH A, SHARIFINIA M. Implications of anthropogenic effects on the coastal environment of Northern Persian Gulf, using Jinga shrimp (Metapenaeus affinis) as indicator[J]. Mar Pollut Bull, 2020, 159: 111463. doi: 10.1016/j.marpolbul.2020.111463
[19] GERAMI M H, GHORBANI R, PAIGHMABARI S Y, et al. Reproductive season, maturation size (LM50) and sex ratio of Metapenaeus affinis (Decapoda: Penaeidae) in Hormozgan shrimp fishing grounds, south of Iran[J]. Int J Aquat Biol, 2013, 1(2): 48-54.
[20] GULNER M, İLKER A. Some reproductive characteristics of Meta-penaeus affinis (H. Milne Edwards, 1837) in Izmir Bay (Eastern Aegean Sea, Turkey)[J]. Pakistan J Zool, 2017, 49(5): 1913-1916.
[21] DASH G, MOHAMMED KOYA K, SEN S, et al. Fishery, population dynamics and stock status of Jinga shrimp, Metapenaeus affinis (H. Milne Edwards, 1837) from Gujarat waters of India[J]. Indian J Geo-Mar Sci, 2018, 47(1): 2267-2277.
[22] ABDEL RAZEK F A, RAGHEB E, EI-DEEB R S, et al. Growth pattern and stock assessment of Jinga shrimp Metapenaeus affinis (H. Milne Edwards, 1837) (Decapoda, Penaeidae) from the southeastern Mediterranean of the Egyptian coasts[J]. Egy J Aquat Res, 2022, 48(1): 83-90. doi: 10.1016/j.ejar.2021.11.008
[23] SAPUTRA S W, SOLICHIN A, TAUFANI W T. Stock Analysis of Metapenaeus affinis (H. Milne Edwards, 1837) on the north coast of central Java, Indonesia[J]. IOP Conf Ser: Earth Environ Sci, 2018, 116(1): 012004.
[24] ZHANG Y, LI Y D, YANG Q B, et al. Transcriptome analysis of Metapenaeus affinis reveals genes involved in gonadal development[J]. Isr J Aquacult-Bamid, 2022, 74: 1722195.
[25] HABIB-UI-HASSAN. Early developmental stages of Metapenaeus affinis (Decapoda, Penaeidae) reared in a laboratory[J]. ICES J Mar Sci, 1980, 39(1): 30-43. doi: 10.1093/icesjms/39.1.30
[26] 江世贵, 杨丛海, 周发林. 等. 斑节对虾种虾繁育技术[M]. 北京: 海洋出版社, 2013: 80-81. [27] ALMAGRO AEMENTEROS J J, TSIRIGOS K D, SØNDERBY C K, et al. SignalP 5.0 improves signal peptide predictions using deep neural networks[J]. Nat Biotechnol, 2019, 37: 420-423. doi: 10.1038/s41587-019-0036-z
[28] CHOU K C, SHEN H B. Cell-PLoc: a package of web servers for predicting subcellular localization of proteins in various organi-sms[J]. Nat Protoc, 2008, 3: 153-162. doi: 10.1038/nprot.2007.494
[29] GUPTA R, BRUNAK S. Prediction of glycosylation across the human proteome and the correlation to protein function[J]. Pac Symp Biocomput. 2002, 7: 310-322.
[30] BLOM N, SICHERITZ-PONTEN T, GUPTA R, et al. Prediction of post-translational glycosylation and phosphorylation of proteins from the amino acid sequence[J]. Proteomics, 2004, 4(6): 1633-1649. doi: 10.1002/pmic.200300771
[31] WILKINS M R, GASTEIGER E, BAIROCH A, et al. Protein identification and analysis tools in the ExPASy server[J]. Methods Mol Biol, 1999, 112: 531-552.
[32] KROGH A, LARSSON B, HEIJINE G V, et al. Sonnhammer: predicting transmembrane protein topology with a hidden markov model: application to complete genomes[J]. J Mol Biol, 2001, 305: 567-580. doi: 10.1006/jmbi.2000.4315
[33] FINN R D, BATEMAN A, CLEMENTS J, et al. Pfam: the protein families database[J]. Nucleic Acids Res, 2014, 42(D1): D222-D230. doi: 10.1093/nar/gkt1223
[34] GEOURJON C, DELEAGE G. SOPM: a self-optimized method for protein secondary structure prediction[J]. Protein Eng, 1994, 7(2): 157-164. doi: 10.1093/protein/7.2.157
[35] WATERHOUSE A, BERTONI M, BIENERT S, et al. SWISS-MODEL: homology modelling of protein structures and complexes[J]. Nucleic Acids Res, 2018, 46(W1): W296-W303. doi: 10.1093/nar/gky427
[36] LARKIN M A, BLACKSHIELDS G, BROWN N P, et al. Clustal W and Clustal X version 2.0[J]. Bioinformatics, 2007, 21(23): 2947-2948.
[37] ROBERT X, GOUET P. Deciphering key features in protein structures with the new ENDscript server[J]. Nucleic Acids Res, 2014, 42(W1): W320-W324. doi: 10.1093/nar/gku316
[38] KUMAR S, STECHER G, TAMURA K. MEGA7: molecular evolutionary genetics analysis version 7.0 for bigger datasets[J]. Mol Biol Evol, 2016, 7(33): 1870-1874.
[39] HILBE J M. A review of current SPSS products: SPSS 12, SigmaPlot 8.02, SigmaStat 3.0, Part 1[J]. Am Stat, 2003, 57(4): 310-315.
[40] EDWARDS P M. Origin 7.0: Scientific graphing and data analysis software[J]. J Chem Inf Comput Sci, 2002, 42(5): 1270-1271. doi: 10.1021/ci0255432
[41] QIAN J, CHEN Y Y, XU Y X, et al. Interactional similarities and differences in the protein complex of PCNA and DNA replication factor C between rice and arabidopsis[J]. BMC Plant Biol, 2019, 19: 257. doi: 10.1186/s12870-018-1600-2
[42] BHARDWAJ V K, PUROHIT R. A new insight into protein-protein interactions and the effect of conformational alterations in PCNA[J]. Int J Biol Macromol, 2020, 148: 999-1009. doi: 10.1016/j.ijbiomac.2020.01.212
[43] YU S M, QIAO X S, YANG Y, et al. The proliferating cell nuclear antigen (PCNA) is a potential proliferative marker in oyster Crassostrea gigas[J]. Fish Shellfish Immunol, 2022, 122: 306-315. doi: 10.1016/j.fsi.2022.02.018
[44] MANSILLA S F, de la VEGA M B, CALZETTA N L, et al. CDK-independent and PCNA-dependent functions of p21 in DNA replication[J]. Genes, 2020, 11(6): 593. doi: 10.3390/genes11060593
[45] FRANCO A, JOUAUX A, MATHIEU M, et al. Proliferating cell nuclear antigen in gonad and associated storage tissue of the Pacific oyster Crassostrea gigas: seasonal immunodetection and expression in laser microdissected tissues[J]. Cell Tissue Res, 2010, 340: 201-210. doi: 10.1007/s00441-009-0923-6
[46] 李治龙. 羽衣甘蓝PCNA基因克隆、亚细胞定位及蛋白表达分析[D]. 哈尔滨: 东北林业大学, 2017: 32-48. [47] MELO R M C, MARTINS Y S, LUZ R K, et al. PCNA and apoptosis during post-spawning ovarian remodeling in the teleost Oreochromis niloticus[J]. Tissue Cell, 2015, 47(6): 541-549. doi: 10.1016/j.tice.2015.10.002
[48] GUZMAN J M, LUCKENBACH J A, YAMAMOTO Y, et al. Expression profiles of fsh-regulated ovarian genes during oogenesis in coho salmon[J]. PLoS One, 2014, 9(12): e114176. doi: 10.1371/journal.pone.0114176
[49] KORFSMEIER K H. PCNA in the ovary of zebrafish (Brachydanio rerio, Ham.- Buch. )[J]. Acta Histochem, 2002, 104: 73-76. doi: 10.1078/0065-1281-00632
[50] LEUNG A Y, LEUNG J C, CHAN L Y, et al. Proliferating cell nuclear antigen (PCNA) as a prolifera-tive marker during embryonic and adult zebrafish hematopoiesis[J]. Histochem Cell Biol, 2005, 124(2): 105-111. doi: 10.1007/s00418-005-0003-2
[51] BALLA M, ANGELOPOULOU R, LAVRANOS G, et al. Follicular cells versus oocytes: cell population dynamics in the developing ovary[J]. Tissue Cell, 2008, 40(5): 373-381. doi: 10.1016/j.tice.2008.03.006
[52] ROA S, AVDIEVICH E, PELED J U, et al. Ubiquitylated PCNA plays a role in somatic hypermutation and class-switch recombina-tion and is required for meiotic progression[J]. Proc Natl Aca Sci, 2008, 105(42): 16248-16253. doi: 10.1073/pnas.0808182105



 下载:
下载:






 粤公网安备 44010502001741号
粤公网安备 44010502001741号
