Establishment of reverse transcription droplet digital PCR assay for detection of Tilapia Lake Virus
-
摘要: 建立一种敏感性高、特异性强、重复性好的罗非鱼湖病毒反转录微滴式数字PCR (RT-ddPCR) 检测方法,可为罗非鱼湖病毒的定量检测提供技术支持。参照NCBI中GenBank登陆的TiLV第3段全基因序列,选择hypothetical protein gene基因作为靶位基因设计合成了1 对引物和探针,以TiLV-cDNA为模板,摸索、优化反应方法,建立与实时荧光RT-PCR检测方法的线性关系,分析方法的敏感性、特异性、重复性,最后进行临床样品检测。结果显示,当引物、探针浓度分别为500、300 nmol·L−1且退火温度为54.2 ℃时,建立的TiLV RT-ddPCR扩增反应效率最高、阴阳性微滴分布界限最明显、平均拷贝数较高;敏感性强,检测限低至2 拷贝·μL−1,且在1~90 000 拷贝·μL−1范围内与实时荧光RT-PCR检测的线性关系较好 (R2=0.995 8);检测变异系数低 (4.86%);与其他5 种常见的水生动物疫病病毒 [鲤浮肿病毒 (Carp edema virus, CEV)、锦鲤疱疹病毒 (Koi herpesvirus, KHV)、草鱼出血病毒 (Grass carp reovirus, GCRV)、鲫造血器官坏死病毒 (Cyprinid herpesvirus 2, CyHV-2)、细胞肿大虹彩病毒 (Red sea bream iridovirus, RSIV)] 阳性样品未发生交叉反应;在临床样品的检测中,48 份罗非鱼样品结果均为阴性,5份能力验证样品中3 份为阳性,与能力验证满意结果一致。
-
关键词:
- 罗非鱼湖病毒 /
- 微滴式逆转录数字PCR /
- 线性关系 /
- 特异性 /
- 变异系数
Abstract: To establish an assay of reverse transcription droplet digital PCR (RT-ddPCR) for Tilapia Lake Virus (TiLV), we designed a pair of specific primers and probe based on the conserved region of TiLV segment 3 and evaluated the specificity, sensitivity and repeatability of this method. The structured standard curve was evaluated by using TiLV-cDNA as a template. Finally, the samples were tested. When the concentrations of primers and probes were 500 and 300 nmol·L−1 and the annealing temperature was 54.2 ℃, the established TiLV RT-ddPCR amplification reaction efficiency was the highest, the distribution boundary of the positive and negative droplets was the most obvious, and the average copy number was higher. The RT-ddPCR of TiLV had a lower limit of detection with 2 copies·μL−1 and showed a good linear relationship between 1–90 000 copies·μL−1 (Correlation coefficient R2=0.995 8). There was no amplification reaction to other viruses in aquatic animals. The CV of ddPCR for TiLV-cDNA was 4.86%. There was no cross reaction with the positive samples of other five common aquatic animal disease viruses [Carp edema virus (CEV), Koi herpesvirus (KHV), Grass carp reovirus (GCV), Cyprinid herpesvirus 2 (CyHV-2), Red sea bream iridovirus (RSIV)]. Among the 53 detected samples, 48 were negative, three of five proficiency testing samples were positive, consistent with satisfactory previous proficiency testing results. -
罗非鱼湖病毒 (Tilapia Lake Virus, TiLV) 是正粘病毒科 (Orthomyxoviridae) 的RNA病毒,罗非鱼的各个生长阶段均可被其感染,死亡率高达90%[1-6]。TiLV的传播途径主要是水平传播,包括直接接触受感染的鱼类[7]、污染的水体及设备[2,7]等,此外,也可能存在垂直传播方式[8]。目前,TiLV已在世界范围内爆发,包括以色列、哥伦比亚、厄瓜多尔、埃及、泰国、印度、马来西亚等国,给全球的罗非鱼养殖产业造成了严重的经济损失[9-15]。虽然至今中国尚无TiLV感染的确切报告,但由于需要从国外引进罗非鱼种苗以保证养殖品质,因此存在境外传入风险。2020 年,中国农业农村部与海关总署联合发布256 号公告,其中将罗非鱼湖病毒病 (Tilapia Lake Virus disease, TiLVD) 列为《中华人民共和国进境动物检疫疫病名录》的二类动物疫病[16]。
目前,国外已相继报道了关于TiLV的电镜观察[9,11,17]、病毒分离培养[5],以及RT-PCR、巢式RT-PCR、半巢式RT-PCR、实时荧光定量RT-PCR等多种核酸的分子生物学检测方法[18-22];国内对于TiLV检测方法的研究相对较晚,且均集中在实时荧光定量RT-PCR方法[23-25]。关于TiLV的逆转录数字PCR检测方法尚未见报道。数字PCR方法作为第三代PCR 技术,其线性数字信号可以提供比实时荧光PCR的指数扩增信号更精确的数据,提高了检测的精度,可以做到绝对定量,已在微生物学研究[26]、食品安全[27-28]、水质监测[29-30]以及登革热[31]、布鲁氏菌 (Brucella spp.)[32]、非洲猪瘟[33]、H5亚型禽流感[34]、牛冠状病毒[35]、马铃薯病毒[36]等有关人、动植物病原体检测等方面应用。本研究参照NCBI中GenBank登陆的TiLV第3 段全基因序列,选择hypothetical protein gene 基因作为靶位基因,设计1 对引物和探针,通过优化反应,建立了RT-ddPCR检测方法,能够准确定量检测罗非鱼湖病毒,有利于加强苗种、养殖、销售等各个环节罗非鱼湖病毒的检测,可为罗非鱼湖病毒相关研究提供参考。
1. 材料与方法
1.1 材料
1.1.1 标准品、样品来源
TiLV标准品购自深圳海关动植物检验检疫技术中心。鲤浮肿病毒 (Carp edema virus, CEV) 、锦鲤疱疹病毒 (Koi herpesvirus, KHV) 、草鱼出血病毒 (Grass carp reovirus, GCRV) 、鲫造血器官坏死病毒 (Cyprinid herpesvirus 2, CyHV-2) 、细胞肿大虹彩病毒 (Red sea bream iridovirus, RSIV)阳性核酸由广东省动物疫病预防控制中心提供。临床样品共53 份,其中5 份为2020 年参加能力验证的验余样品 (源自深圳海关动植物检验检疫技术中心) ,其余48 份采自东莞市罗非鱼养殖场。
1.1.2 主要试剂
总RNA提取试剂盒、FastKing一步法除基因组cDNA第一链合成预混试剂均购自天根;ddPCR Supermix for Probes (No dUTP) 、微滴生成油均购自Bio-Rad;引物、探针由生工生物工程 (上海) 股份有限公司合成;PBS溶液由东莞市动物疫病预防控制中心实验室配制;其他试剂 (无水乙醇、氯仿) 为分析纯。
1.1.3 仪器设备
生物安全柜 (Class II BSC,新加坡ESCO科技有限公司);生物样品均质器 (Precelly Evolution,法国BERTIN);普通 PCR 仪、数字 PCR 系统 QX200、96孔板封口机 PX1 (Bio-Rad 公司);荧光PCR仪 (AFD4800,杭州安杰思医学科技有限公司)。
1.1.4 引物、探针的设计
参照NCBI中GenBank登陆的TiLV第3段全基因序列,选择hypothetical protein gene 基因作为靶位基因,引物、探针序列详见表1。
表 1 RT-ddPCR和实时荧光RT-PCR检测罗非鱼湖病毒的引物、探针Table 1. Primer and probe of RT-ddPCR and real-time RT-PCR for TiLV detection引物、探针 Primer, probe 引物序列 (5'—3')Primer sequence (5'–3') 上游引物Upstream primer TTCGAGTGCTCAAAGTTCCT 下游引物 Downstream primer CGTGCGTACTCGTTCAGTATA 探针 Probe FAM-TCAAGACCACACTCCTCACCRCAG-BHQ1 1.2 方法
1.2.1 临床样品的前处理
本研究所用的48 份临床样品采自东莞市罗非鱼养殖场。取罗非鱼的肝、脾内脏置于2 mL研磨管中,加入1 mL PBS溶液,放入生物样品均质器 (转速7 200 r·min−1;匀浆4 次,每次15 s,每次间隔30 s) 进行匀浆,离心后备用。
1.2.2 RNA提取和cDNA模板制备
TiLV标准品和临床样品,首先根据总RNA提取试剂盒的操作说明书提取RNA,然后对提取的罗非鱼湖病毒和草鱼出血热病毒RNA进行逆转录。逆转录反应体系为20 μL,其中包括,5×FastKing-RT SuperMix 4 μL,Total RNA 2 μL,RNase-Free ddH2O 14 μL。逆转录反应程序为:42 ℃去除基因组及反转录15 min;95 ℃酶灭活3 min。
1.2.3 TiLV-cDNA ddPCR方法的建立
参考ddPCR Supermix for Probes说明书配制反应体系,同时设阴性对照和空白对照。20 μL ddPCR反应体系生成微滴后转移至96 孔板,置于PCR仪进行扩增,完成后放入微滴读取仪,读取结束后分析结果。ddPCR的反应体系和反应程序见表2。
表 2 TiLV-cDNA ddPCR反应体系和反应程序Table 2. Reaction mixture and protocol of ddPCR for TiLV-cDNA detection反应体系Reaction mixture 用量 Volume/mL 终浓度Final concentration 反应程序 Protocol 温度Temperature/℃ 时间Time 循环次数Cycle 2×ddPCR SupermixTM for Probes 10 1× 95 10 min 1 引物 Primer 0.36 900 nmol·L−1 94 30 s 40 探针 Probe 0.1 250 nmol·L−1 60 60 s 1 cDNA模板 cDNA template 1.0 — 98 10 min 1 双蒸水 ddH2O 8.18 — 4 ∞ — 1.2.4 反应条件的优化
选用 TiLV-cDNA的4 倍稀释梯度为模板,对ddPCR反应条件进行优化,包括探针、引物浓度和退火温度。优化的关键因素是最大限度地提高阴性和阳性微滴分区之间的荧光振幅差异且最小化具有中等荧光强度的分区数量。1) 优化探针浓度:设置了4组探针浓度进行ddPCR 反应,分别为150、200、250、300 nmol·L−1,每组设3个重复。2) 优化引物浓度:最优探针浓度确定后,设定上、下游引物终浓度分别为 200、300、400、500、600、700、800、900 、1 000、1 100、1 200 nmol·L−1时进行 ddPCR 反应,每组设3个重复。3) 优化退火温度:引物、探针的最优浓度确定后,退火温度设为61.0、60.2、58.8、56.7、54.2、52.1、50.8和50.0 ℃,每个退火温度设置 3 个重复。
1.2.5 标准曲线的建立
用ddH2O对TiLV-cDNA进行2 倍系列稀释,共20 个梯度,每个梯度进行3 次重复试验,同时进行ddPCR和实时荧光PCR检测。设立阴性对照和空白对照。以ddPCR测定的各梯度TiLV-cDNA的分子数的对数lg值为横坐标,荧光PCR检测的Ct值为纵坐标,构建标准曲线。实时荧光PCR总反应体系为 25 μL,其中包括,5×PCR buffer 5 μL,dNTPs 2 μL,Taq DNA聚合酶 0.6 μL,上下游引物 (500 nmol·L−1) 各 0.1 μL,探针 (500 nmol·L−1) 0.08 μL,cDNA模板 2 μL,ddH2O 15.12 μL。实时荧光PCR反应程序为 95℃ 3 min;95℃ 15 s,55℃ 30 s (收集荧光), 45 个循环。引物、探针序列见表1。
1.2.6 特异性试验
按优化后的1.2.3 项对CEV、KHV、GFHNV、RSIV、GCRV、TiLV的DNA或cDNA进行检测,评估本研究建立的TiLV-cDNA ddPCR的特异性。
1.2.7 重复性试验
按优化后的1.2.3 项对4 倍稀释度的TiLV-cDNA进行检测,设15 个重复,计算变异系数,以评估本研究建立的TiLV-cDNA ddPCR的稳定性。
1.2.8 临床样品的检测
用建立的RT-ddPCR方法对48 份罗非鱼肝脾的核酸样品和5 份能力验证样品进行检测。
1.3 统计学方法
TiLV-cDNA的ddPCR数据使用Quantasoft软件进行图像处理和结果分析。以微滴生成总数大于10 000 个作为ddPCR试验成立的标准。同时阴性对照和空白对照中没有检测到阳性微滴,表明该体系没有被污染或特异性扩增。所有微滴经PCR扩增后,包含靶标的微滴有扩增,其荧光强度较高判为阳性微滴,不包含靶标的微滴未扩增,荧光强度较低判为阴性微滴。因此,经过微滴读取仪判读后,微滴总体会有一个阳性率值p,结合泊松分布算法,每个阳性微滴的拷贝数为−ln (1−p) ,同时,每个微滴体积固定且已知,则可换算得到样品每微升拷贝数的浓度值。实验数据以“平均值±标准差 (
$\overline { X}\pm { \rm {SD} }$ )”表示,用SPSS 16.0软件进行处理,在单因子方差 (One-way ANOVA) 分析的基础上,采用Duncan's多重比较检验组间差异,以P<0.05作为差异显著的标准。cDNA分子数=每微升拷贝数(拷贝·μL−1) ×20 μL ddPCR反应体系/cDNA模板用量。2. 结果
2.1 RT-ddPCR方法的建立
2.1.1 探针浓度的优化
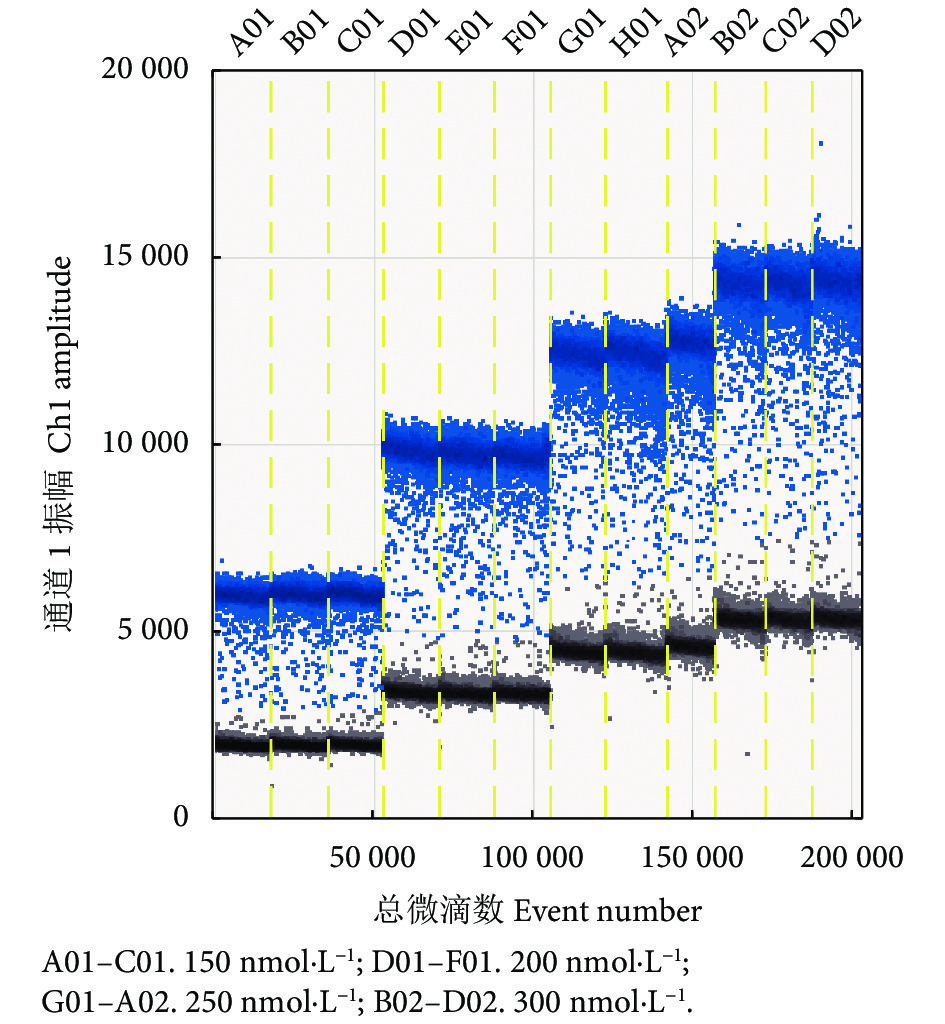
不同浓度探针的ddPCR扩增的微滴生成数目均大于15 000 个,结果成立。不同探针浓度间的cDNA分子数依次是150 nmol·L−1组>300 nmol·L−1组>200 nmol·L−1组>250 nmol·L−1组,且不存在显著性差异 (P>0.05,表3) 。当探针浓度为150 nmol·L−1时,cDNA分子数最大,但是ddPCR反应的荧光强度最低且阴性和阳性微滴分区之间的荧光振幅差异最小,不符合优化的判定标准。当探针浓度达到 300 nmol·L−1时,荧光强度最大,获得了最大效率的扩增反应,阳性微滴与阴性微滴分布的界限最为明显。综合判断,当引物浓度为900 nmol·L−1、退火温度为60 ℃时,探针最优浓度是300 nmol·L−1 (表3,图1) 。
表 3 不同探针浓度的ddPCR检测的cDNA分子数Table 3. Normalized detected target DNA by ddPCR at different probe concentrations探针浓度Probe concentration/ (nmol·L−1) cDNA分子数Normalized detected target DNA/ (拷贝·μL−1) 150 16 400±1 624.84 200 16 040±1 020.89 250 15 060±1 175.79 300 16 080±1 561.57 2.1.2 引物浓度的优化
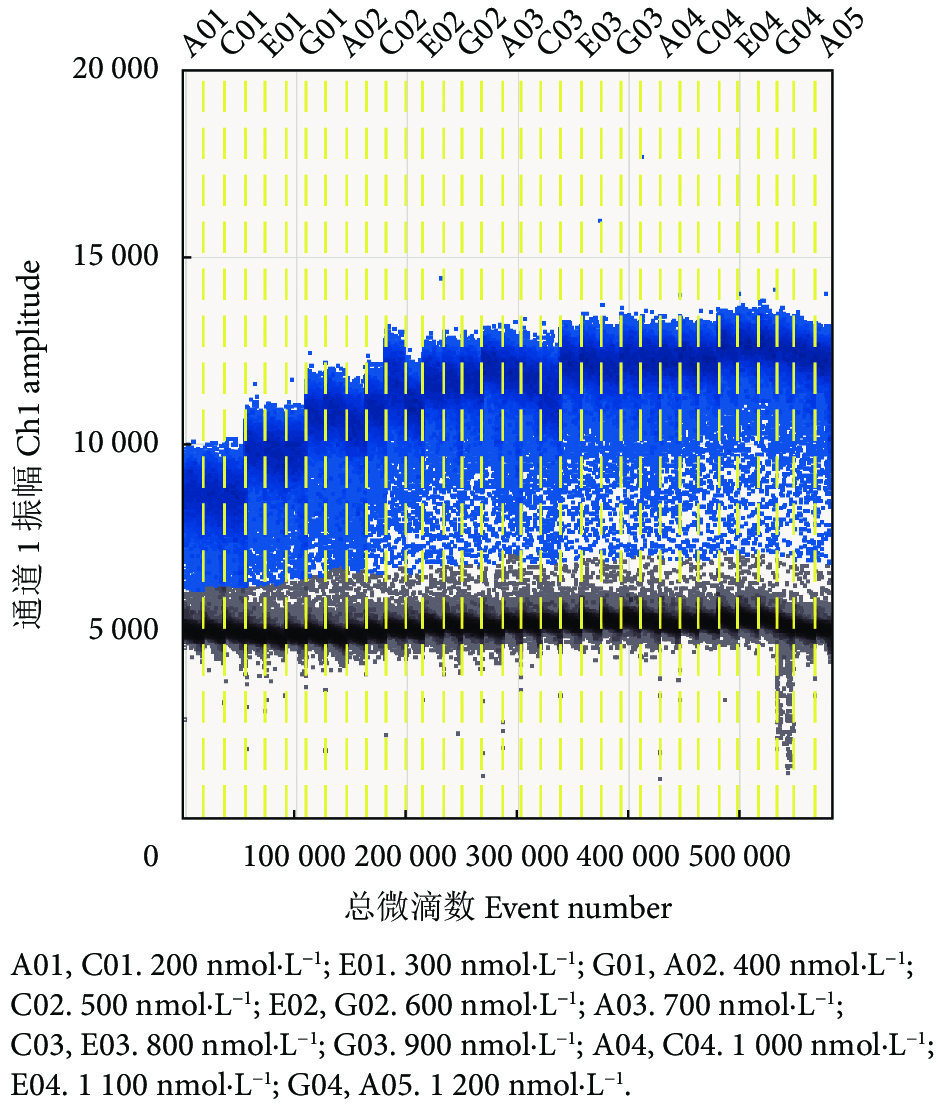
探针浓度为300 nmol·L−1时,不同引物浓度间的cDNA分子数由大到小依次为:900 nmol·L−1组>500 nmol·L−1组>600 nmol·L−1组>800 nmol·L−1组>1 000 nmol·L−1组>300 nmol·L−1组>400 nmol·L−1组>700 nmol·L−1组>1 200 nmol·L−1组>1 100 nmol·L−1组>200 nmol·L−1组,但无显著性差异 (P>0.05) 。当引物终浓度为 500 nmol·L−1时,能获得最大效率的扩增反应,阳性微滴与阴性微滴分布的界限明显。因此,当退火温度为60 ℃时,引物最优浓度为500 nmol·L−1 (表4,图2) 。
表 4 不同引物浓度的ddPCR检测的cDNA分子数Table 4. Normalized detected target cDNA by ddPCR at different primer concentrations引物浓度Primer concentration/(nmol·L−1) cDNA分子数Normalized detected target DNA/(拷贝·μL−1) 200 15 580±1 165.28 300 16 540±2 645.52 400 16 500±900.57 500 17 360±336.39 600 16 800±331.46 700 16 440±507.02 800 16 760±131.99 900 17 500±861.06 1 000 16 720±244.59 1 100 15 620±1 082.75 1 200 15 760±1 268.10 2.1.3 退火温度的优化
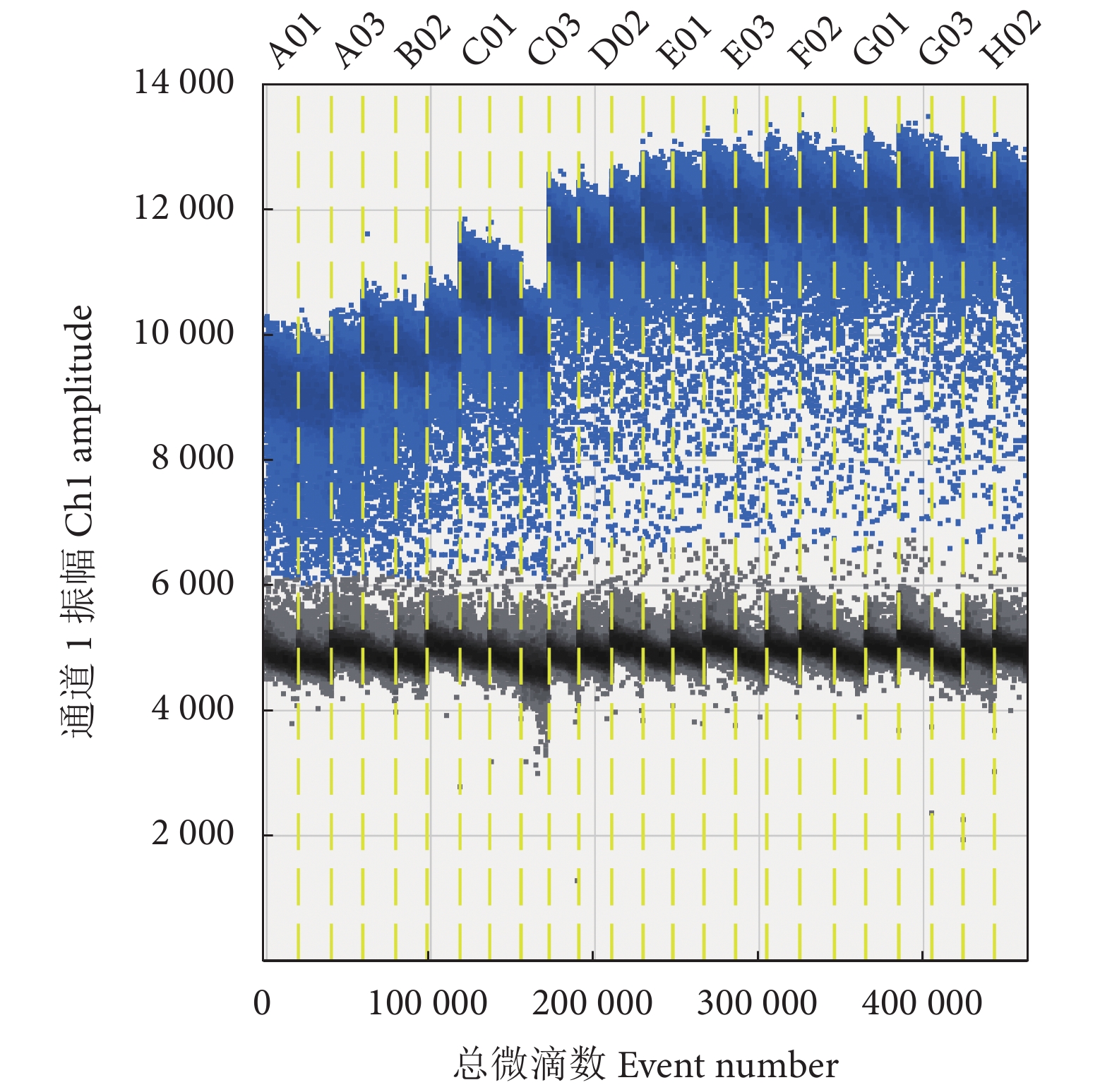
引物、探针浓度分别为500、300 nmol·L−1时,退火温度设为61、60.2、58.8、56.7、54.2、52.1、50.8和50 ℃进行ddPCR 反应。结果显示:不同退火温度的ddPCR扩增的微滴生成数目均大于15 000,结果成立。不同退火温度间的cDNA分子数由大到小依次为54.2 ℃组>61 ℃组>50.8 ℃组>52.1 ℃组>56.7 ℃组>58.8 ℃组>50 ℃组>60.2 ℃组,且无显著性差异 (P>0.05) 。当退火温度为54.2 ℃时,能获得最大效率的扩增反应,阳性微滴和阴性微滴分布界限最为明显,且平均拷贝数最高 (16 360 拷贝·μL−1),因此,最优退火温度是54.2 ℃ (表5,图3) 。
表 5 不同退火温度ddPCR检测的cDNA分子数Table 5. Normalized detected target cDNA by ddPCR at different annealing temperatures退火温度Annealing temperature/℃ cDNA分子数Normalized detected target DNA/ (拷贝·μL−1) 61.0 16 280±1 420.83 60.2 15 140±2 237.92 58.8 15 780±4 166.57 56.7 15 980±1 908.79 54.2 16 360±2 022.83 52.1 16 020±2 432.50 50.8 16 260±1 830.22 50.0 15 740±1 942.53 2.2 标准曲线的构建
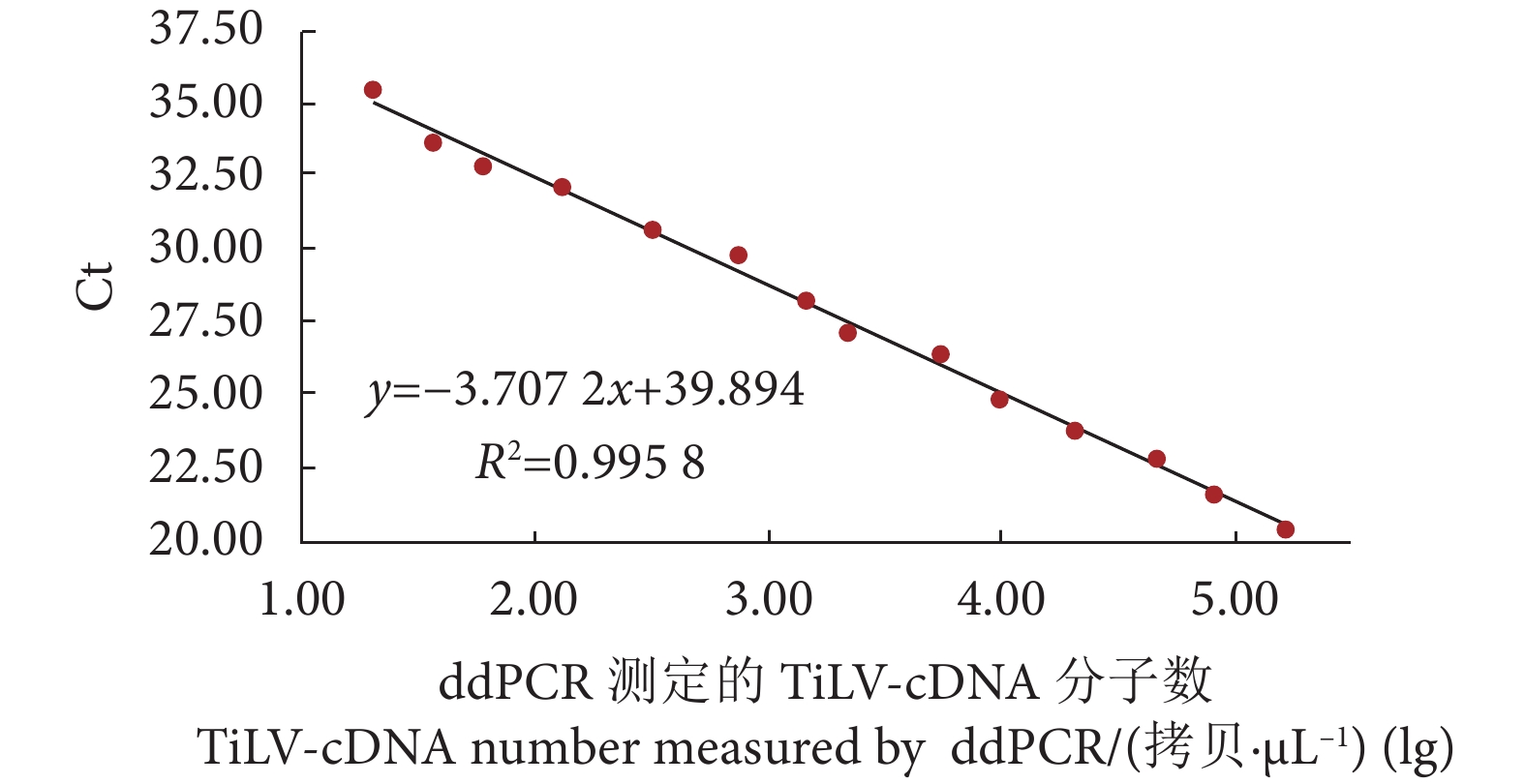
20 个不同梯度的TiLV-cDNA进行ddPCR试验,扩增的微滴生成数目均大于13 000 个,结果成立。ddPCR检测的平均下限为2 拷贝·μL−1,实时荧光PCR的检测下限为3.6 拷贝·μL−1,ddPCR的灵敏度高于实时荧光PCR方法 (表6) 。以ddPCR测定的各梯度TiLV-cDNA的分子数的lg值为横坐标,实时荧光PCR检测的Ct值为纵坐标,构建标准曲线。不同梯度ddPCR在检测范围内具有极好的相关性,y= −3.707 2x+39.894,R2=0.995 8。在进行临床样品检测时,可根据此标准曲线来计算该样品的核酸分子数 (图4) 。
表 6 TiLV-cDNA ddPCR和实时荧光PCR方法敏感性试验Table 6. Sensitivity test of ddPCR and real-time PCR for TiLV-cDNA微滴式数字 PCR ddPCR 实时荧光 PCR real-time PCR 样品/稀释倍数Sample/Dilution ratio 总微滴数*Number of droplets 阳性微滴数*Positive droplets cDNA分子数Normalized detected target DNA/(拷贝·μL−1) cDNA分子数的平均值±标准差$\overline { X}\pm { \rm {SD}}$ cDNA分子数的变异系数CV/% Ct值Ct value 平均值±标准差$\overline { X}\pm { \rm {SD}}$ 变异系数CV/% cDNA 15 547 15 023 79 800 82 800±4 233.20 5.11 20.12 20.41±0.37 1.83 18 355 17 778 81 400 20.83 17 782 17 357 87 800 20.27 cDNA/2 17 010 13 679 38 360 40 880±3 070.53 7.51 21.75 21.60±0.17 0.80 17 982 15 251 44 340 21.41 17 358 14 207 40 140 21.63 cDNA/4 18 420 11 442 22 840 23 220±340.78 1.47 23.13 22.81±0.45 1.97 17 543 11 058 23 420 23.01 18 527 11 687 23 440 22.3 cDNA/8 19 145 6 374 9 520 10 360±3 731.40 36.02 24.05 23.78±0.28 1.16 19 992 7 041 4 220 23.79 18 496 7 108 1 1420 23.5 cDNA/16 19 583 3 906 5 240 5 002±274.95 5.50 24.94 24.86±0.40 1.61 19 997 3 870 5 060 24.43 19 031 3 845 4 700 25.22 cDNA/32 18 624 2 007 2 740 2 736±170.10 6.22 26.32 26.39±0.22 0.85 18 828 1 946 2 560 26.64 18 722 2 176 2 900 26.21 cDNA/64 18 708 757 972 1 092±120.01 10.99 26.79 27.15±0.33 1.20 18 944 858 1 090 27.25 18 618 935 1 212 27.42 cDNA/128 17 010 525 738 738±11.02 1.49 28.41 28.24±0.32 1.14 17 723 556 750 28.44 18 609 567 728 27.87 cDNA/256 18 922 320 402 374±27.15 7.26 29.73 29.78±0.24 0.80 17 785 277 370 30.04 16 723 245 348 29.57 cDNA/512 17 195 134 184 162±19.70 12.16 30.81 30.67±0.19 0.63 13 343 88 156 30.75 16 586 103 146 30.45 cDNA/1 024 18 273 55 70 66±5.29 8.01 32.11 32.10±0.01 0.03 17 070 49 68 32.1 17 303 44 60 32.09 cDNA/2 048 17 316 23 32 29.8±8.84 29.66 32.74 32.86±0.15 0.47 18 791 30 38 32.8 18 324 16 20.6 33.03 cDNA/4 096 18 590 15 19 18.4±0.42 2.26 33.39 33.68±0.46 1.36 16 562 13 18.4 34.21 16 821 13 18.2 33.44 cDNA/8 192 17 892 4 5.2 10.2±5.10 50.00 35.99 35.44±0.61 1.73 16 910 11 15.4 35.55 16 276 7 10.2 34.78 cDNA/16 384 17 413 4 5.4 6.2±0.69 11.17 38.95 37.01±1.70 4.59 17 684 5 6.6 36.27 17 941 5 6.6 35.8 cDNA/32 768 17 761 4 5.2 3.6±1.45 40.18 38.55 37.95±0.73 1.92 18 207 2 2.6 38.16 17 341 2 2.8 37.14 cDNA/65 536 17 395 1 1.4 2±0.60 30.00 18 230 2 2.6 16 999 1 2 cDNA/131 072 18 359 0 0 18 619 0 0 14 472 0 0 cDNA/262 144 15 121 0 0 14 538 0 0 13 526 0 0 cDNA/524 288 15 733 0 0 14 537 0 0 15 672 0 0 注:*. 20 μL反应体系。 Note: *. 20 μL reaction mixture. 2.3 特异性试验
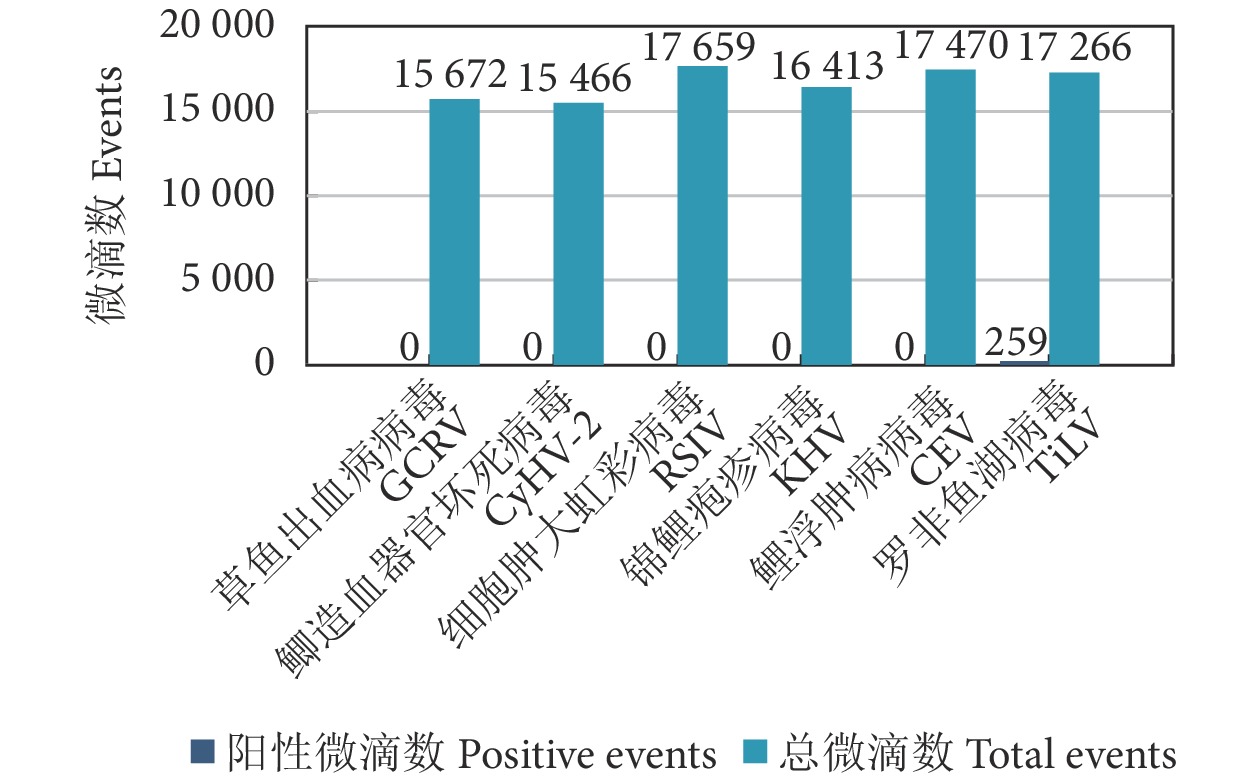
建立的TiLV-cDNA ddPCR方法分别对CEV、KHV、GFHNV、RSIV的DNA和GCRV、TiLV的cDNA进行特异性试验。结果显示,ddPCR扩增的微滴生成数目均大于15 000 个,结果成立。除了TiLV阳性样本出现了阳性微滴 (259个) ,其他5 种阳性病毒核酸检测均未出现阳性微滴。说明建立的RT-ddPCR检测方法对TiLV具有较好的特异性 (图5)。
2.4 重复性试验
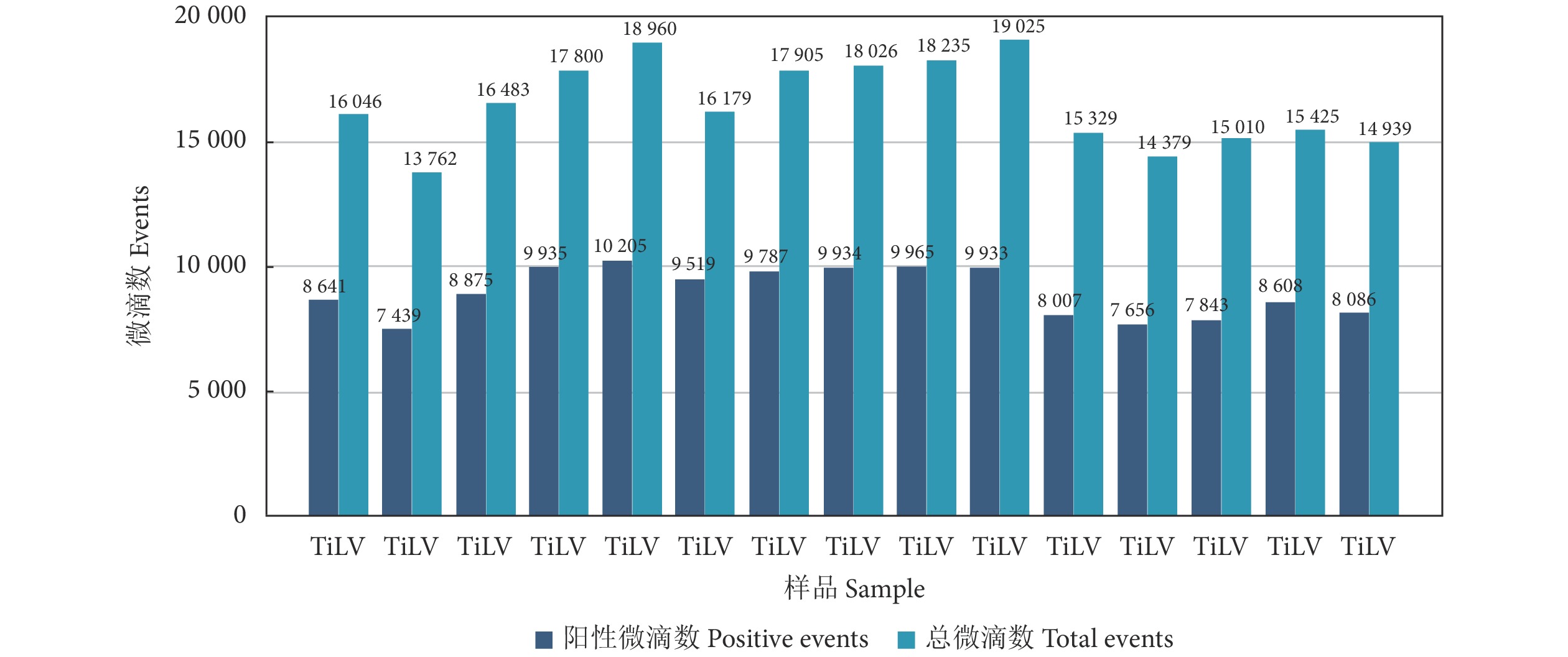
选用将4 倍稀释的TiLV-cDNA作为大于17 000 个,结果成立。组内试验的变异系数 (CV) 为4.86%,证明建立的TiLV RT-ddPCR具有良好的重复性 (表7,图6) 。
表 7 4倍稀释的TiLV-cDNA ddPCR组内重复性试验Table 7. Replicate of intra-assay for 4-fold dilution of TiLV-cDNA ddPCR样品编号Sample No. cDNA分子数Normalized detected target DNA/(拷贝·μL−1) TiLV-1 18 200 TiLV-2 18 300 TiLV-3 18 200 TiLV-4 19 220 TiLV-5 18 180 TiLV-6 20 880 TiLV-7 18 620 TiLV-8 18 840 TiLV-9 18 600 TiLV-10 17 380 TiLV-11 17 380 TiLV-12 17 880 TiLV-13 17 400 TiLV-14 19 220 TiLV-15 18 340 平均数±标准差 $\overline { X}\pm { \rm {SD}}$ 18 442.67±896.15 变异系数 CV/% 4.86 2.5 临床样品的检测
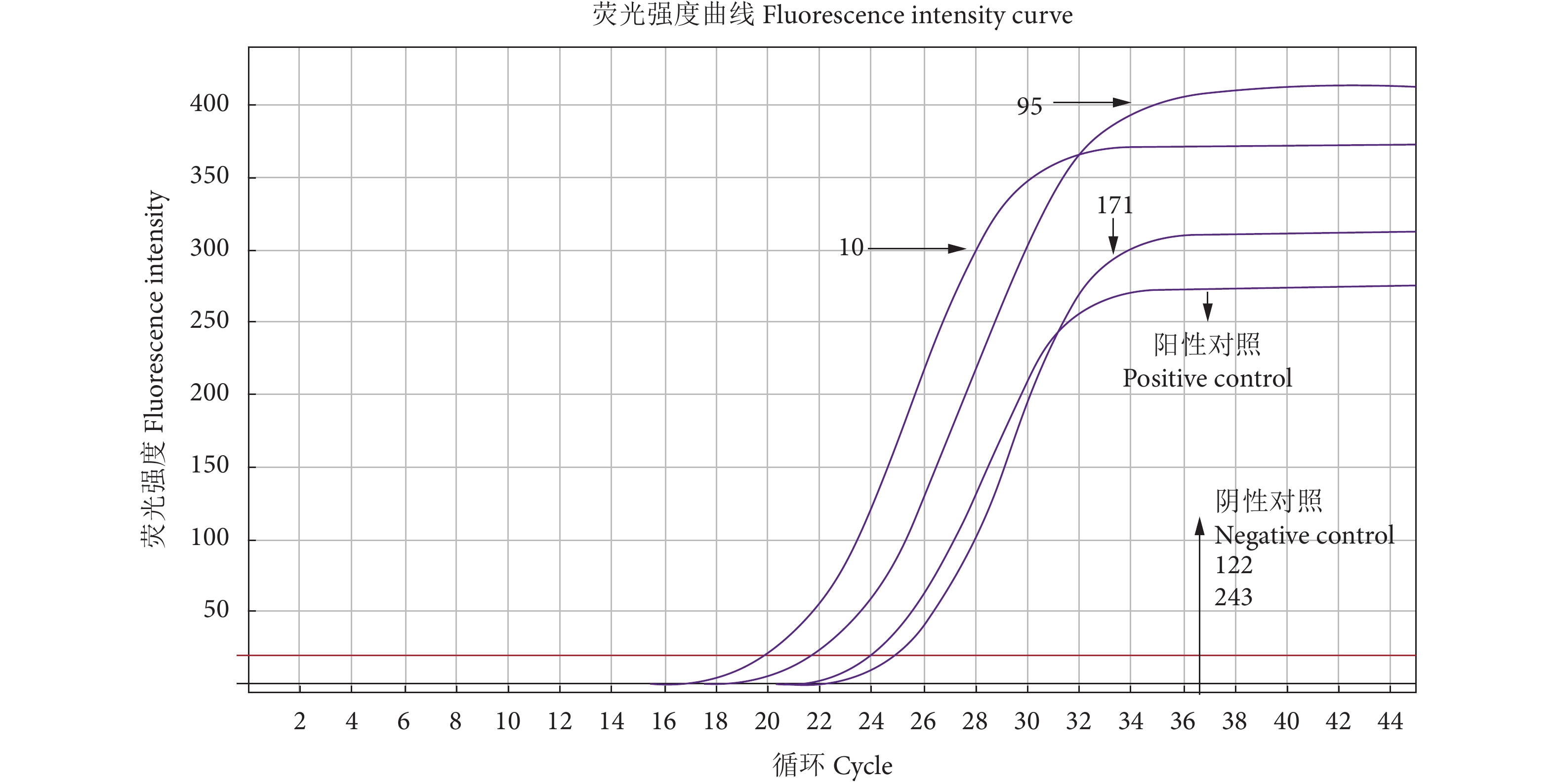
利用建立的TiLV RT-ddPCR方法对5 份能力验证样品和48 份罗非鱼临床样品进行检测,RT-ddPCR扩增的微滴生成数目均大于12 000 个,结果成立。48 份罗非鱼样品均为阴性,5份能力验证样品中检出阳性样品3 份,与2020年能力验证满意结果一致 (表8,图7—图8)。3 份阳性样品的病毒核酸检测结果分别为17 760、1 920、518 拷贝·μL−1。说明建立的RT-ddPCR方法可行性好,适合于临床样品的检测和标准样品的标定。
表 8 TiLV (能力验证样品) RT-ddPCR与实时荧光RT-PCR检测结果Table 8. Results of TiLV RT-ddPCR and real-time RT-PCR for proficiency testing samples能力验证样品编号No. of proficiency testing sample cDNA分子数Normalized detected target DNA/(拷贝·μL−1) Ct值*Ct value 10 17 760 19.90 95 1 920 21.58 122 0 Undet 171 518 24.85 243 0 Undet 注:*. 实时荧光RT-PCR方法 (SC/T 7223—2020)。 Note: *. Real-time RT-PCR (SC/T 7223—2020). 3. 讨论
TiLV可以感染各个生长阶段的罗非鱼且发病快、死亡率高,目前尚没有针对TiLV的疫苗。在感染的早期阶段,鱼类体内的病毒含量较低,容易被忽略,因此更需要特异性强、敏感性高的检测方法。2014 年,Eyngor等[2]在罗非鱼原代脑细胞和E-11细胞系中成功分离出TiLV,并首次建立了RT-PCR检测方法,检测到TiLV的节段3,该段被国际病毒分类委员会 (The International Committee on Taxonomy of Viruses, ICTV) 单列为罗非鱼湖病毒种[37-38]。世界范围内爆发的TiLV病毒株之间同源性很高,说明TiLV在遗传进化过程中序列相对保守、变异小[39]。本研究根据NCBI中GenBank登陆的TiLV第3 段全基因序列,选择hypothetical protein gene 基因作为靶位基因,设计了1 对引物、探针并建立了TiLV RT-ddPCR检测方法,是世界上的首次报道,本方法特异性强且最低检测病毒分子数为2 拷贝·μL−1,敏感性高于国内外目前已建立的其他分子生物学检测方法[18-25]。
巢氏/半巢氏RT-PCR只能用于定性检测并且操作时间长,EB (或EB代替染料) 的使用也会给操作人员及环境带来污染风险;实时荧光RT-PCR依赖标准曲线和Ct值,并且也不能直观表示检测对象的病毒含量;ddPCR是第三代PCR,无需标准曲线,基本上总是产生对反应中目标拷贝的直接估计,具有定量核酸的能力,其线性数字信号可以提供比实时荧光PCR的指数扩增信号更精确的数据,提高了检测的精度。由于ddPCR提供了高水平的精度和检测核酸分子量的微小差异,近年来,ddPCR技术的应用进展广泛且多样,但是关于水生动物疫病的ddPCR的研究目前只有鲤疱疹病毒2型[40-42]、传染性鲑鱼贫血病毒[43]等疫病的应用。
本研究以TiLV-cDNA为模板,引物、探针浓度分别为500、300 nmol·L−1,退火温度为54.2 ℃时,能获得最大效率的扩增反应,阳性微滴和阴性微滴分布的界限最为明显。试验发现,本研究建立的TiLV RT-ddPCR的组内CV值为4.86%,表明本方法的稳定性好。在1~90 000 拷贝·μL−1范围内,ddPCR最低可检出2 拷贝·μL−1,实时荧光PCR方法最低可检出3.6 拷贝·μL−1。两种方法在检测范围内线性关系良好,y= −3.707 2x+39.894,R2=0.995 8。因此,本研究建立的TiLV RT-ddPCR特异性强、敏感性高、重复性好,可以在鱼类感染TiLV的早期阶段进行临床诊断,可为罗非鱼的进出口贸易安全提供保障。
本研究在样品提取RNA 后,首先将其反转录为cDNA,这样操作的目的是cDNA比RNA更容易保存,在温度低于−20 ℃条件下可长期保存;此外,还可以节约检测试剂成本,一步法的RT-ddPCR反应体系的检测成本远高于ddPCR反应体系,并且经过前期一步法的RT-ddPCR反应体系检测结果与反转录后的ddPCR检测比对,差异不显著。本研究建立的TiLV RT-ddPCR可以做到绝对定量,对标准样品和质控品的标定具有重要意义,也为今后TiLV标准样品的研制和标定提供了绝对定量检测技术。
-
表 1 RT-ddPCR和实时荧光RT-PCR检测罗非鱼湖病毒的引物、探针
Table 1 Primer and probe of RT-ddPCR and real-time RT-PCR for TiLV detection
引物、探针 Primer, probe 引物序列 (5'—3')Primer sequence (5'–3') 上游引物Upstream primer TTCGAGTGCTCAAAGTTCCT 下游引物 Downstream primer CGTGCGTACTCGTTCAGTATA 探针 Probe FAM-TCAAGACCACACTCCTCACCRCAG-BHQ1 表 2 TiLV-cDNA ddPCR反应体系和反应程序
Table 2 Reaction mixture and protocol of ddPCR for TiLV-cDNA detection
反应体系Reaction mixture 用量 Volume/mL 终浓度Final concentration 反应程序 Protocol 温度Temperature/℃ 时间Time 循环次数Cycle 2×ddPCR SupermixTM for Probes 10 1× 95 10 min 1 引物 Primer 0.36 900 nmol·L−1 94 30 s 40 探针 Probe 0.1 250 nmol·L−1 60 60 s 1 cDNA模板 cDNA template 1.0 — 98 10 min 1 双蒸水 ddH2O 8.18 — 4 ∞ — 表 3 不同探针浓度的ddPCR检测的cDNA分子数
Table 3 Normalized detected target DNA by ddPCR at different probe concentrations
探针浓度Probe concentration/ (nmol·L−1) cDNA分子数Normalized detected target DNA/ (拷贝·μL−1) 150 16 400±1 624.84 200 16 040±1 020.89 250 15 060±1 175.79 300 16 080±1 561.57 表 4 不同引物浓度的ddPCR检测的cDNA分子数
Table 4 Normalized detected target cDNA by ddPCR at different primer concentrations
引物浓度Primer concentration/(nmol·L−1) cDNA分子数Normalized detected target DNA/(拷贝·μL−1) 200 15 580±1 165.28 300 16 540±2 645.52 400 16 500±900.57 500 17 360±336.39 600 16 800±331.46 700 16 440±507.02 800 16 760±131.99 900 17 500±861.06 1 000 16 720±244.59 1 100 15 620±1 082.75 1 200 15 760±1 268.10 表 5 不同退火温度ddPCR检测的cDNA分子数
Table 5 Normalized detected target cDNA by ddPCR at different annealing temperatures
退火温度Annealing temperature/℃ cDNA分子数Normalized detected target DNA/ (拷贝·μL−1) 61.0 16 280±1 420.83 60.2 15 140±2 237.92 58.8 15 780±4 166.57 56.7 15 980±1 908.79 54.2 16 360±2 022.83 52.1 16 020±2 432.50 50.8 16 260±1 830.22 50.0 15 740±1 942.53 表 6 TiLV-cDNA ddPCR和实时荧光PCR方法敏感性试验
Table 6 Sensitivity test of ddPCR and real-time PCR for TiLV-cDNA
微滴式数字 PCR ddPCR 实时荧光 PCR real-time PCR 样品/稀释倍数Sample/Dilution ratio 总微滴数*Number of droplets 阳性微滴数*Positive droplets cDNA分子数Normalized detected target DNA/(拷贝·μL−1) cDNA分子数的平均值±标准差$\overline { X}\pm { \rm {SD}}$ cDNA分子数的变异系数CV/% Ct值Ct value 平均值±标准差$\overline { X}\pm { \rm {SD}}$ 变异系数CV/% cDNA 15 547 15 023 79 800 82 800±4 233.20 5.11 20.12 20.41±0.37 1.83 18 355 17 778 81 400 20.83 17 782 17 357 87 800 20.27 cDNA/2 17 010 13 679 38 360 40 880±3 070.53 7.51 21.75 21.60±0.17 0.80 17 982 15 251 44 340 21.41 17 358 14 207 40 140 21.63 cDNA/4 18 420 11 442 22 840 23 220±340.78 1.47 23.13 22.81±0.45 1.97 17 543 11 058 23 420 23.01 18 527 11 687 23 440 22.3 cDNA/8 19 145 6 374 9 520 10 360±3 731.40 36.02 24.05 23.78±0.28 1.16 19 992 7 041 4 220 23.79 18 496 7 108 1 1420 23.5 cDNA/16 19 583 3 906 5 240 5 002±274.95 5.50 24.94 24.86±0.40 1.61 19 997 3 870 5 060 24.43 19 031 3 845 4 700 25.22 cDNA/32 18 624 2 007 2 740 2 736±170.10 6.22 26.32 26.39±0.22 0.85 18 828 1 946 2 560 26.64 18 722 2 176 2 900 26.21 cDNA/64 18 708 757 972 1 092±120.01 10.99 26.79 27.15±0.33 1.20 18 944 858 1 090 27.25 18 618 935 1 212 27.42 cDNA/128 17 010 525 738 738±11.02 1.49 28.41 28.24±0.32 1.14 17 723 556 750 28.44 18 609 567 728 27.87 cDNA/256 18 922 320 402 374±27.15 7.26 29.73 29.78±0.24 0.80 17 785 277 370 30.04 16 723 245 348 29.57 cDNA/512 17 195 134 184 162±19.70 12.16 30.81 30.67±0.19 0.63 13 343 88 156 30.75 16 586 103 146 30.45 cDNA/1 024 18 273 55 70 66±5.29 8.01 32.11 32.10±0.01 0.03 17 070 49 68 32.1 17 303 44 60 32.09 cDNA/2 048 17 316 23 32 29.8±8.84 29.66 32.74 32.86±0.15 0.47 18 791 30 38 32.8 18 324 16 20.6 33.03 cDNA/4 096 18 590 15 19 18.4±0.42 2.26 33.39 33.68±0.46 1.36 16 562 13 18.4 34.21 16 821 13 18.2 33.44 cDNA/8 192 17 892 4 5.2 10.2±5.10 50.00 35.99 35.44±0.61 1.73 16 910 11 15.4 35.55 16 276 7 10.2 34.78 cDNA/16 384 17 413 4 5.4 6.2±0.69 11.17 38.95 37.01±1.70 4.59 17 684 5 6.6 36.27 17 941 5 6.6 35.8 cDNA/32 768 17 761 4 5.2 3.6±1.45 40.18 38.55 37.95±0.73 1.92 18 207 2 2.6 38.16 17 341 2 2.8 37.14 cDNA/65 536 17 395 1 1.4 2±0.60 30.00 18 230 2 2.6 16 999 1 2 cDNA/131 072 18 359 0 0 18 619 0 0 14 472 0 0 cDNA/262 144 15 121 0 0 14 538 0 0 13 526 0 0 cDNA/524 288 15 733 0 0 14 537 0 0 15 672 0 0 注:*. 20 μL反应体系。 Note: *. 20 μL reaction mixture. 表 7 4倍稀释的TiLV-cDNA ddPCR组内重复性试验
Table 7 Replicate of intra-assay for 4-fold dilution of TiLV-cDNA ddPCR
样品编号Sample No. cDNA分子数Normalized detected target DNA/(拷贝·μL−1) TiLV-1 18 200 TiLV-2 18 300 TiLV-3 18 200 TiLV-4 19 220 TiLV-5 18 180 TiLV-6 20 880 TiLV-7 18 620 TiLV-8 18 840 TiLV-9 18 600 TiLV-10 17 380 TiLV-11 17 380 TiLV-12 17 880 TiLV-13 17 400 TiLV-14 19 220 TiLV-15 18 340 平均数±标准差 $\overline { X}\pm { \rm {SD}}$ 18 442.67±896.15 变异系数 CV/% 4.86 表 8 TiLV (能力验证样品) RT-ddPCR与实时荧光RT-PCR检测结果
Table 8 Results of TiLV RT-ddPCR and real-time RT-PCR for proficiency testing samples
能力验证样品编号No. of proficiency testing sample cDNA分子数Normalized detected target DNA/(拷贝·μL−1) Ct值*Ct value 10 17 760 19.90 95 1 920 21.58 122 0 Undet 171 518 24.85 243 0 Undet 注:*. 实时荧光RT-PCR方法 (SC/T 7223—2020)。 Note: *. Real-time RT-PCR (SC/T 7223—2020). -
[1] 胡虎子, 曾伟伟, 王英英, 等. 罗非鱼湖病毒病研究进展[J]. 病毒学报, 2020, 36(1): 145-154. doi: 10.13242/j.cnki.bingduxuebao.003629 [2] EYNGOR M, ZAMOSTIANO R, KEMBOU T J E, et al. Identification of a novel RNA virus lethal to tilapia[J]. J Clin Microbiol, 2014, 52(12): 4137-4146. doi: 10.1128/JCM.00827-14
[3] JANSEN M D, MOHAN C V. Tilapia lake virus (TiLV): literature review[R]. Penang: CGIAR Research Program on Fish Agri-Food Systems, 2017: 1-11.
[4] DONG H T, SIRIROOB S, MEEMETTA W, et al. Emergence of tilapia lake virus in Thailand and an alternative semi nested RT-PCR for detection[J]. Aquaculture, 2017, 476: 111-118. doi: 10.1016/j.aquaculture.2017.04.019
[5] BEHERA B K, PRADHAN P K, SWAMINATHAN T R, et al. Emergence of tilapia lake virus associated with mortalities of farmed Nile tilapia Oreochromis niloticus (Linnaeus 1758) in India[J]. Aquaculture, 2018, 484: 168-174. doi: 10.1016/j.aquaculture.2017.11.025
[6] SURACHETPONG W, JANETANAKIT T, NONTHABENJAWAN N, et al. Outbreaks of tilapia lake virus infection, Thailand, 2015–2016[J]. Emerging Infect Dis, 2017, 23(6): 1031-1033. doi: 10.3201/eid2306.161278
[7] LIAMNIMITR P, THAMMATORN W, U-THOOMPORN S, et al. Non-lethal sampling for tilapia lake virus detection by RT-qPCR and cell culture[J]. Aquaculture, 2018, 486: 75-80. doi: 10.1016/j.aquaculture.2017.12.015
[8] NICHOLSON P, FATHI M A, FISCHER A, et al. Detection of tilapia lake virus in Egyptian fish farms experiencing high mortalities in 2015[J]. J Fish Dis, 2017, 40(12): 1925-1928. doi: 10.1111/jfd.12650
[9] FERGUSON H W, KABUUSU R, BELTRAN S, et al. Syncytial hepatitis of farmed tilapia, Oreochromis niloticus(L. ): a case report[J]. J Fish Dis, 2014, 37(6): 583-589. doi: 10.1111/jfd.12142
[10] BACHARACH E, MISHRA N, BRIESE T, et al. Characterization of a novel rthomyxo-like virus causing mass die-offs of tlapia[J]. mBio, 2016, 7(2): e00431-e00416.
[11] DEL-POZO J, MISHRA N, KABUUSU R, et al. Syncytial hepatitis of tilapia (Oreochromis niloticus L. ) is associated with Orthomyxovirus-like virions in hepatocytes[J]. Vet Pathol, 2017, 54(1): 164-170. doi: 10.1177/0300985816658100
[12] FATHI M, DICKSON C, DICKSON M, et al. Identification of tilapia lake virus in Egypt in Nile tilapia affected by "summer mortality" syndrome[J]. Aquaculture, 2017, 473: 430-432. doi: 10.1016/j.aquaculture.2017.03.014
[13] AICH N, PAUL A, CHOUDHURY T G, et al. Tilapia Lake Virus (TiLV) disease: current status of understanding[J]. Aquac Fish, 2022, 7(1): 7-17.
[14] AMAL M N A, KOH C B, NURLIYANA M, et al. A case of natural co-infection of tilapia lake virus and Aeromonas veronii in a Malaysian red hybrid tilapia (Oreochromis niloticus×O. mossambicus) farm experiencing high mortality[J]. Aquaculture, 2018, 485(2): 12-16.
[15] JAEMWIMOL P, RAWIWAN P, TATTIYAPONG P, et al. Susceptibility of important warm water fish species to tilapia lake virus (TiLV) infection[J]. Aquaculture, 2018, 497(1): 462-468.
[16] 郑晓聪, 黄倩君, 朱崧琪, 等. 罗非鱼湖病毒病传入风险分析[J]. 中国动物检疫, 2020, 37(10): 27-31. doi: 10.3969/j.issn.1005-944X.2020.10.006 [17] TATTIYAPONG P, DACHAVICHITLEAD W, SURACHETPONG W. Experimental infection of tilapia lake virus (TiLV) in Nile tilapia (Oreochromis niloticus) and red tilapia (Oreochromis spp.)[J]. Vet Microbiol, 2017, 207: 170-177. doi: 10.1016/j.vetmic.2017.06.014
[18] TSOFACK J E K, ZAMOSTIANO R, WATTED S, et al. Detection of tilapia lake virus in clinical samples by culturing and nested reverse transcription-PCR[J]. J Clin Microbiol, 2017, 55(3): 759-767. doi: 10.1128/JCM.01808-16
[19] DONG H T, ATAGUBA G A, KHUNRAE P, et al. Evidence of TiLV infection in tilapia hatcheries from 2012 to 2017 reveals probable global spread of the disease[J]. Aquaculture, 2017, 479: 579-583. doi: 10.1016/j.aquaculture.2017.06.035
[20] TATTIYAPONG P, SIRIKANCHANA K, SURACHETPONG W. Development and validation of a reverse transcription quantitative polymerase chain reaction for tilapia lake virus detection in clinical samples and experimentally challenged fish[J]. J Fish Dis, 2018, 41(2): 255-261. doi: 10.1111/jfd.12708
[21] WAIYAMITRA P, TATTIYAPONG P, SIRIKANCHANA K, et al. A TaqMan RT-qPCR assay for tilapia lake virus (TiLV) detection in tilapia[J]. Aquaculture, 2018, 497: 184-188. doi: 10.1016/j.aquaculture.2018.07.060
[22] YIN J Y, WANG Q, WANG Y Y, et al. Development of a simple and rapid reverse transcription-loopmediated isothermal amplification (RT-LAMP) assay for sensitive detection of tilapia lake virus[J]. J Fish Dis, 2019, 42(6): 817-824. doi: 10.1111/jfd.12983
[23] 雷燕, 肖洋, 赵振峰, 等. 罗非鱼罗湖病毒RT-PCR检测方法的建立及初步应用[J]. 广东海洋大学学报, 2019, 39(3): 1-5. doi: 10.3969/j.issn.1673-9159.2019.03.001 [24] 吴凤雷, 黄瑜, 黄郁葱, 等. 罗湖病毒实时荧光定量RT-PCR检测方法的建立[J]. 广东海洋大学学报, 2019, 39(5): 31-37. [25] 徐淑菲, 朱黄鑫, 增韵颖, 等. 罗湖病毒 (TiLV) RT-PCR方法的建立[J]. 渔业研究, 2022, 44(2): 154-161. [26] KIM T G, JEONG S Y, CHO K S. Comparison of droplet digital PCR and quantitative real-time PCR for examining population dynamics of bacteria in soil[J]. Appl Microbiol Biot, 2014, 98(13): 6105-6113. doi: 10.1007/s00253-014-5794-4
[27] MORISSET D, STEBIH D, MILAVEC M, et al. Quantitative analysis of food and feed samples with droplet digital PCR[J]. PLoS One, 2013, 8(5): e62583. doi: 10.1371/journal.pone.0062583
[28] FLOREN C, WIEDEMANN I, BRENIG B, et al. Species identification and quantification in meat and meat products using droplet digital PCR (ddPCR)[J]. Food Chem, 2015, 173: 1054-1058. doi: 10.1016/j.foodchem.2014.10.138
[29] RACKI N, DREO T, GUTIERREZ-AGUIRRE I, et al. Reverse transcriptase droplet digital PCR shows high resilience to PCR inhibitors from plant, soil and water samples[J]. Plant Methods, 2014, 10(1): 42. doi: 10.1186/s13007-014-0042-6
[30] CAO Y P, RAITH M R, GRIFFIFITH J F. Droplet digital PCR for simultaneous quantification of general and human-associated fecal indicators for water quality assessment[J]. Water Res, 2015, 70: 337-349. doi: 10.1016/j.watres.2014.12.008
[31] MAIRIANG D, SONGJAENG A, HANSUEALUEANG P, et al. Application of one-step reverse transcription droplet Digital PCR for dengue virus detection and quantification in clinical specimens[J]. Diagnostics, 2021, 11(4): 639. doi: 10.3390/diagnostics11040639
[32] 董浩, 原霖, 刘洋, 等. 布氏杆菌微滴数字 PCR 方法的建立[J]. 畜牧与兽医, 2022, 54(2): 97-101. [33] 邬旭龙, 肖璐, 宋勇, 等. 非洲猪瘟病毒微滴数字PCR (ddPCR)方法的建立及应用[J]. 微生物学通报, 2017, 44(12): 2839-2846. [34] 刘琳. H5亚型AIV实时荧光RT-PCR、数字PCR方法建立及HA单抗的重组表达[D]. 北京: 中国农业科学院, 2020: 19-25. [35] 马义诚. 牛冠状病毒微滴式数字PCR检测方法的建立及应用[D]. 乌鲁木齐: 新疆农业大学, 2021: 25-41. [36] 张永江, 黄洁芳, 王溪桥, 等. 微滴数字PCR (ddPCR)检测马铃薯S病毒 (PVS)[J]. 农业生物技术学报, 2017, 25(10): 1721-1728. [37] ADAMS M J, LEFKOWITZ E J, KING A M, et al. Changes to taxonomy and the international code of virus classification and nomenclature ratified by the international committee on taxonomy of viruses[J]. Arch Virol, 2017, 162(8): 2505-2538. doi: 10.1007/s00705-017-3358-5
[38] CHENGULA A A, MUTOLOKI S, EVENSEN Ø, et al. Tilapia lake virus does not hemagglutinate avian and piscine erythrocytes and NH4Cl does not inhibit viral replication in vitro[J]. Viruses, 2019, 11(12): 1152. doi: 10.3390/v11121152
[39] 熊敏思. 2017 年 FAO 全球渔业回顾及展望[J]. 渔业信息与战略, 2018, 33(1): 71-74. [40] 赵欣, 贾鹏, 刘莹, 等. 鲤疱疹病毒2型微滴式数字PCR检测方法的建立及比较分析[J]. 渔业科学进展, 2017, 38(4): 126-133. [41] 郝中香, 林华, 佘容, 等. 鲤疱疹病毒2型微滴式数字PCR快速检测方法的建立[J]. 中国兽医科学, 2016, 46(2): 167-173. doi: 10.16656/j.issn.1673-4696.2016.02.006 [42] 郝中香. 异育银鲫CyHV-2检测方法的建立及江淮主产区CyHV-2感染的分子流行病学调查[D]. 成都: 四川农业大学, 2016: 25-33. [43] WELI S C, BERNHARDT L V, QVILLER L, et al. Infectious salmon anemia virus shedding from infected Atlantic salmon (Salmo salar L.): application of a droplet digital PCR assay for virus quantification in seawater[J]. Virus, 2021, 13(9): 1770. doi: 10.3390/v13091770
-
期刊类型引用(3)
1. 肇慧君,胡强,于灵,吴斌,易佳颖. 病毒性出血性败血症病毒数字PCR检测方法的建立. 水产科学. 2024(01): 111-120 .  百度学术
百度学术
2. 胡毅军,丁文桂,黄洁莹,罗律,赖颖,王自强,李敏,张险朋. 罗非鱼链球菌检测方法研究进展. 中国动物检疫. 2024(01): 80-86 .  百度学术
百度学术
3. 叶毅飞,梁国华,吴志鹏,殷进方,龙海鹰,周柱辉,莫钻兰,邓海燕,谢翠美,林其明,李敏,张险朋. 迟缓爱德华氏菌荧光PCR方法的建立及初步应用. 中国动物检疫. 2024(09): 89-96 .  百度学术
百度学术
其他类型引用(2)



 下载:
下载:


 粤公网安备 44010502001741号
粤公网安备 44010502001741号
